При плавлении солей карбоновых кислот со щелочами образуются сответственные предельные углеводороды,поэтому выйдет такое уравнение:
4,8 г 3,6 г
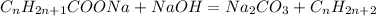
40 г х г
1. Найдем молекулярную массу углеводорода:
при взаимодействии 4,8 г гидроксида образуется 3,6 г углеводорода, а
при --//--//-- 40 г___________________х г, откуда
х=40*3,6/4,8=30 г
2. Зная общую формулу предельных углеводородов и подставив эту массу(цифру) в формулу по вычислению относительной молекулярной массы,получим уравнение: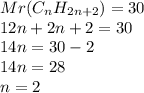 ,значит формула углеводорода:
,значит формула углеводорода: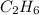 - это этан
- это этан
ответ:Задание 1.
Сходства:
они расположили химические элементы в порядке возрастания их атомных масс.
Различия:
Дёберейнер : он их объединил в 1829 году.
Он заметил что некоторые сходные по своим свойствам элементы можно объединить по три в группы.
Он назвал их триадами.
Система классификации Дёберейнер оказалась несовешенной.
Ньюлендс: он их объединил в 1865 году 18 августа.
Он заметил что каждый восьмой элемент напоминает по свойствам первый элемент.
Назвал он такую закономерность законом октав.
Менделеев: он их объединил в марте 1869 года.
Менделеев предсказывает существование трёх ещё неизвестных элементов.
Задание 2.
Вывод:
Вклад Дёберейнера: Он заметил что некоторые по своим свойствам элементы можно объединить по три группы. он назвал их триадами. Он был первым естествоиспытателей, который взял Свойства химических элементов с их атомными массами.
Вклад Ньюлендса: он расположил химические элементы в порядке возрастания их атомных масс. в результате он заметил, что каждый восьмой элемент напоминает по свойствам первый элемент. найденную закономерность, он назвал законом октав по аналогии с семью интервалами музыкальной в 1879 году открыл скадий.
Вклад Менделеева: в 1869 году русский Химик Менделеев представил русскому химическим обществу значение открытия им периодического закона химических элементов. В том же году вышло первое издание Менделеева учебника "основы химии" , в котором были приведено его периодическая таблица. В конце 1870 года Менделеев делает доклад по русскому химическому обществу под названием " Естественные системы химических элементов и применение её указанию свойств еще неизвестных элементов". В этом докладе он рассказывает о существование ещё 3 неизвестных элементов: экасилиций, экабор и экаалюминий.
Объяснение:
Уже конечно поздно, но это может пригодится другим.
Надеюсь я сделала все правильно,делала все по тексту.
Объяснение:
удачи)
4NH3+5O2-->4NO+6H2O
V=6,0 л
n(количество вещества)=
=v/Vm=6,0 л/ 22,4 л/моль=0,27 моль
По соотношению молейn(NH3):n(NO)=4:4=1:1 => n(NO)=0,27 моль=> V(NO)=n*Vm=0,27 моль*22,4 л/моль=6,048 л
Так же n(NH3):n(O2)=4:5 , по пропорции 4:5=0,27 моль:х=>x=0,34 моль( количество вещества O2) V=n*Vm=0,34 моль*22,4 л /моль=7.616 л