22,4
Объяснение:
Дано:
m(CaO) = 112 г
Найти:
V(O₂) = ?
Реакция: 2Ca + O₂ → 2CaO
Сначала находим количество вещества оксида кальция:
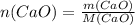 , где M(CaO) - молярная масса CaO, которая считается как сумма атомных масс Ca и O (даны в таблице Менделеева)
, где M(CaO) - молярная масса CaO, которая считается как сумма атомных масс Ca и O (даны в таблице Менделеева)
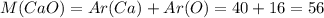 г/моль
г/моль
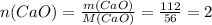 моль
моль
По реакции видно, что оксида кальция в 2 раза больше, чем затраченного кислорода (по коэффициентам смотрим: у CaO 2, у O₂ 1). Поэтому и количество вещества у кислорода будет в 2 раза меньше, чем у оксида кальция:
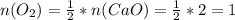 моль
моль
Объем считаем по формуле:
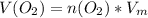 , где
, где 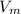 - молярный объем, который для всех газов при н.у. равен 22,4 л/моль.
- молярный объем, который для всех газов при н.у. равен 22,4 л/моль.
Подставляем и решаем:
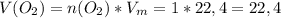 л
л
ответ: 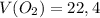 л
л
m1 (р-ра) = 400г
W1 = 25% = 0.25
W2 = 20% = 0.2
Найти:
V (H2) - ?
Решение:
m (сахарозы) = W1 * m1 (p-pa) = 0.25 * 400 = 100г
m2 (раствора) = m1 (раствора) + m (H2O)
W2 = m (сахарозы) / m2 (раствора)
0.2 = 100 / (400 + m (H2O))
100 = 0.2 * (400 + m (H2O))
100 = 80 + 0.2 * m (H2O)
0.2 * m (H2O) = 20
m (H2O) = 20 / 0.2 = 100г
V (H2O) = m (H2O) / p (H2O) = 100 / 1 = 100 мл = 0.1 л
ответ: V (H2O) = 0.1 л