1) 6I₂ + 12NaOH →10 NaI + 2NaIO₃ + 6H₂O ; реакция диспропорционирования
2) 2KMnO4 + 5H₂O₂ + 3H₂SO₄ → 2MnSO₄ + 5O₂ + K₂SO₄ +8H₂O ; межмолекулярная ОВР
Объяснение:
1) I₂ + NaOH → NaI + NaIO₃ + H₂O
5|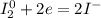 - восстановление (окислитель - I₂)
- восстановление (окислитель - I₂)
1|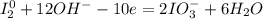 - окисление (восстановитель - I₂)
- окисление (восстановитель - I₂)

Добавляем к каждому аниону натрий:
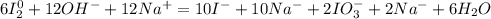
Получаем:
6I₂ + 12NaOH →10 NaI + 2NaIO₃ + 6H₂O
Тип ОВР - реакция диспропорционирования (I₂ выступает и в роли окислителя, и в роли восстановителя)
2) KMnO4 + H₂O₂ + H₂SO₄ → MnSO₄ + O₂ + K₂SO₄ +H₂O
2| - восстановление (окислитель - KMnO4)
- восстановление (окислитель - KMnO4)
5| - окисление (восстановитель - H₂O₂ )
- окисление (восстановитель - H₂O₂ )
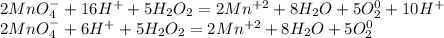
Добавляем к каждому аниону калий, а катиону - SO₄:

Получаем:
2KMnO4 + 5H₂O₂ + 3H₂SO₄ → 2MnSO₄ + 5O₂ + K₂SO₄ +8H₂O
Тип ОВР - межмолекулярная ОВР (окислитель и восстановитель - разные вещества)
Відповідь:
Дополнение к заданию по ЭДС
Пояснення:
Чтобы определить ЭДС реакции, нужно найти разность потенциала окислителя и потенциала восстановителя
Значения стандартных электродных потенциалов берем из справочной таблицы
ЭДС = Е⁰ок — Е⁰восст
Е⁰ (Н⁺/Н⁰) = 0 окислитель
Е⁰ (Cr⁺³/Cr⁰) = -0,740 восстановитель
ЭДС = Е⁰ (Н⁺/Н⁰) - Е⁰ (Cr⁺³/Cr⁰) = 0 - ( -0,740) = 0,740
Е⁰ (Н⁺/Н⁰) = 0 окислитель
Е⁰)Al⁺³/Al⁰) = - 1,660 восстановитель
ЭДС = Е⁰ (Н⁺/Н⁰) - Е⁰)Al⁺³/Al⁰) = 0 - ( - 1,660) = 1,660
Реакции могут протекать в прямом направлении, т.к. их ЭДС > 0.
ответ:
1,2,3
объяснение:
обычно так бензин разводят
2.lто фильтр
3.это в ст машинке