1) ковалентная-неполярная связь между двумя сходными неметаллами:
ответ: 4
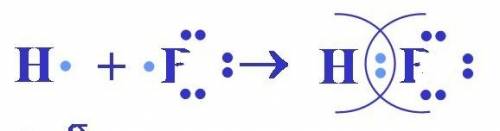
2) ковалентная-полярная связь между двумя разными неметаллами:
ответ: 2
3) наибольшая электроотрицательность у неметаллов:
ответ: 4
4) 1 --б 2 --- в 3---4
5) схема в фото. тип связи: ковалентно-неполярная
6) схема в фото. тип связи: ковалентно-полярная
2в комментарии как у 1 варианта
1) ответ: 3
2) ответ: 1
3) ответ: 3
4) 1 --- б 2-- в 4--а
1) схема в фото. тип связи: ковалентно-неполярная
2) схема в фото. тип связи: ковалентно-полярная
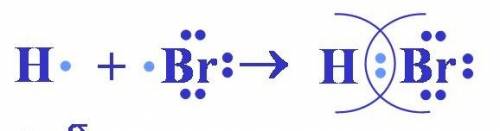
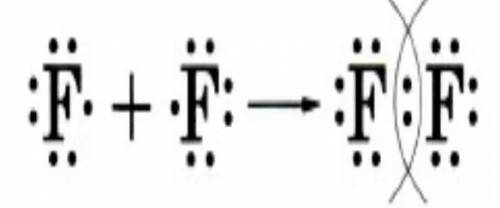
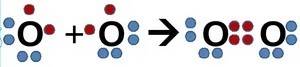
1) Определим массу 1 моля безводного Na₂SO₃ и кристаллогидрата Na₂SO₃*10Н₂О:
М(Na₂SO₃) = 2*23 + 32 + 3*16 = 126 г/моль
М(Na₂SO₃*10Н₂О) = 126 + 10*18 = 306 г/моль
2) Тогда массовая доля безводного Na₂SO₃ в его кристаллогидрате составляет:
ω = 126/306 = 0,4118
3) Если концентрация раствора выражена в долях единицы, то массу растворенного вещества в граммах находят по формуле:
m(в-во) = ω * m(p-p)
где: m(p-p) - масса раствора в граммах, ω - массовая доля растворенного вещества, выраженная в долях единицы.
4) Обозначим массу кристаллогидрата через Х, а так как масса растворенного вещества не изменяется, то можем составить уравнение:
0,4118*Х = 0,1 * (Х + 800)
0,3118Х = 80
Х = 256,57
ответ: 256,57 г
1.
P2O5 - P V, O II
SO3 - S VI, O II
PH3 - P III, H I
N2O5 - N V, O II
2. CrF3, BaO, CoBr2
3. Mr(Li2S) = Ar(S) + 2Ar(Li) = 1 * 32 + 2 * 7 = 46
4.
Mr(CaO) = Mr = Ar(O) + Ar(Ca) = 1 * 16 + 1 * 40 = 56
w(O) = Ar(O) / Mr = 16 / 56 = 0.2857 = 28.57 %
5.
2Na + 2HCl = 2NaCl + H2 - замещения
K2O + H2O = 2KOH - соединения
H2SO4 + MgO = MgSO4 + H2O - обмена