2H3PO4+6NaOH->2Na3PO4+6H2O
Образовалась соль - ортофосфат натрия
2H3PO4+6KOH->2K3PO4+6H2O
Образовалась соль - ортофосфат калия
H3PO4+3NH4OH->(NH4)3PO4+2H2O
Образовалась соль - ортофосфат аммония.
2H3PO4+3Cu(OH)2->Cu3(PO4)2+6H2O
Образовалась соль - ортофосфат меди
2H3PO4+3Fe(OH)2->Fe3(PO4)2+6H2O
Образовалась соль - ортофосфат железа
H3PO4+Al(OH)3->AlPO4+3H2O
Образовалась соль - ортофосфат алюминия.
2H3PO4+3CaO->Ca3(PO4)2+3H2O
Образовалась соль - ортофосфат кальция
2H3PO4+3BaO->Ba3(PO4)2+3H2O
Образовалась соль - ортофосфат бария
2H3PO4+3MgO->Mg3(PO4)2+3H2O
Образовалась соль - ортофосфат магния
2H3PO4+3Na2O->2Na3PO4+3H2O
Образовалась соль - ортофосфат натрия
2H3PO4+3K2O->2K3(PO4)+3H2O
Образовалась соль - ортофосфат калия.
Дано:
m(раствора H₂SO₄)=490г.
ω%(H₂SO₄)=10%
---------------------------
m(BaSO₄)-?
1. Определим массу серной кислоты в растворе :
ω%=m(вещества)÷m(раствора NaOH)×100%
m(H₂SO₄)=ω%(H₂SO₄)×m(раствора H₂SO₄)÷100%
m(H₂SO₄)=10%×490г÷100%=49г.
2. Определим молярную массусерной кислоты и ее количество вещества в 49г.:
M(H₂SO₄)=98г./моль
n(H₂SO₄)=m(H₂SO₄)÷M(H₂SO₄)=49г.÷98г./моль=0,5моль
3. Запишем уравнение реакции:
H₂SO₄ + Ba(NO₃)₂ = BaSO₄↓ + 2HNO₃
n(H₂SO₄)=n(BaSO₄)=1моль
n₁(H₂SO₄)=n₁(BaSO₄)=0,5моль
4. Определим молярную массу сульфата бария и его массу количеством вещества 0,5моль:
M(BaSO₄)=137+32+64=233г./моль
M(BaSO₄)=n₁(BaSO₄)хM(BaSO₄)=0,5мольх233г./моль=116,5г.
5. ответ: смешивании раствора массой 490г. с массовой долей серной кислоты 10% с достаточным количеством раствора барий нитрата образовался осадок сульфата бария массой 116,5г.
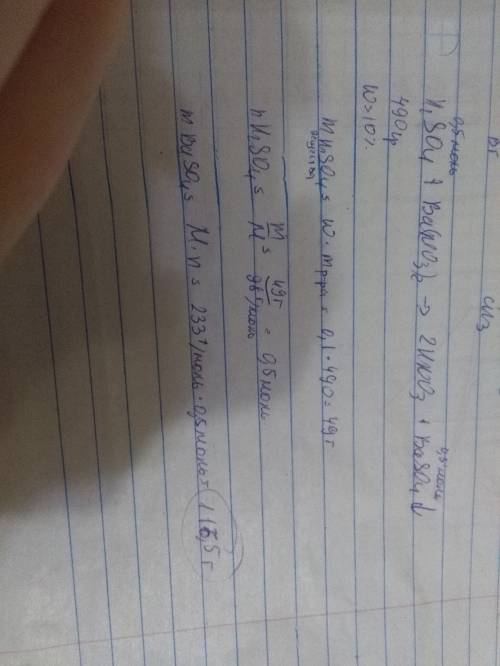
5KNO3+K2SO4+2MnSO4+3H2O
N(+3)-2e=N(+5) 5 ок-ие
в-ль
Mn(+7)+5e=Mn(+2) 2. в-ие
ок-ль