Объяснение:
V = 120 мл
См = 0,1 М
m(NaCl) --- ? г
Решение
0,1 М означает, что в 1 литре раствора содержится 0,1 моля вещества
M(NaCl) = 23 + 35,5 = 58,5 (г/моль)
0,1 М = 58,5 : 10 = 5,85 (г/л)
Нужную массу хлорида натрия находим, составляя пропорцию:
1000 мл ----- 5,85 г NaCl
120 мл ---- х г NaCl
х = 5,85 * 120/1000 = 0,702 г
ответ: 0,702 г
Примечание. Для расчета необходимой массы вещества (г) для приготовления нужного объема (мл) его раствора заданной молярности можно воспользоваться формулой:
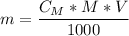
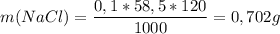
Объяснение:
V = 120 мл
См = 0,1 М
m(NaCl) --- ? г
Решение
0,1 М означает, что в 1 литре раствора содержится 0,1 моля вещества
M(NaCl) = 23 + 35,5 = 58,5 (г/моль)
0,1 М = 58,5 : 10 = 5,85 (г/л)
Нужную массу хлорида натрия находим, составляя пропорцию:
1000 мл ----- 5,85 г NaCl
120 мл ---- х г NaCl
х = 5,85 * 120/1000 = 0,702 г
ответ: 0,702 г
Примечание. Для расчета необходимой массы вещества (г) для приготовления нужного объема (мл) его раствора заданной молярности можно воспользоваться формулой:
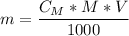
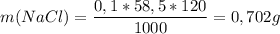
V(CO)=1,8л
Vm=22,4л./моль
m(Fe)-?
1.Определим количество вещества оксида углерода(ll) в его 1,8л.:
n(CO)=V(CO)÷Vm=1,8л ÷ 22,4л./моль=0,08моль
2. Запишем уравнение реакции взаимодействия оксида углерода(ll) с оксидом железа(lll):
Fe₂O₃ + 3CO = 2Fe + 3CO₂
3. Анализируем уравнение реакции: по уравнению реакции из 3моль оксида углерода(ll) образуется 2моль железа. По условию задачи 0,08моль оксида углерода(ll), значит образуется количество вещества железа: n(Fe)=0,08моль х2моль÷3моль=0,05моль.
4. Находим молярную массу железа и его массу количеством вещества 0,05моль:
M(Fe)=56г./моль
m(Fe) = n(Fe)×M(Fe)= 0,05моль ×56г./моль=2,8г.
5. ответ: при действии угарного газа 1,8л. на оксид железа(lll), образуется железо массой 2,8г.