Объяснение:
Электронный слой (в англ. electron shell) - это совокупность электронов одного энергетического уровня (совокупность электронов, имеющих одинаковое значение n - главного квантового числа).
Или условно выражаясь, электронный слой - это энергетический уровень, на котором есть хотя бы один электрон.
Поэтому можно сказать к примеру, что в атоме водорода один электронный слой (но не один энергетический уровень, энергетических уровней там много), или номер периода равен количеству электронных слоёв в атоме (но не номер периода равен количеству энергетических уровней в атоме).
Задание 1.
Названия бинарных соеденинений:
Ca3N2 - нитрид кальция;
Al4C3 - карбид алюминия;
CaH2 - гидрид кальция;
FeO - оксид железа (||);
K2S - сульфид кальция;
MgCl2 - хлорид магния;
Na3P - фосфид натрия;
PH3 - фосфин или фосфид водорода.
Степени окисления:
Ca(+2)N(-3)
Al(-3)C(+4)
Ca(+2)H(-1) - пример исключения, когда водород приобретает степень окисления -1
Fe(+2)O(-2) - тоже пример исключения (довольно частый), когда кислород приобретает степень окисления -2.
K(+1)S(-2)
Mg(+2)Cl(-2)
Na(+1)P(-3)
P(+3)H(-1)
Задание 2.
Дано: m(CO2)= 14(г)
Найти: V(CO2)=? (л)
Формулы
m=n*M
V=n*Vm
постоянная величина, которая нам всегда известна Vm=22,4 (л/моль)
1) n(CO2)= m(CO2) : M(CO2)= 14 (г) : (12+16*2) (г/моль) = 0,3 (моль)
2) V(CO2)= n(CO2) * Vm = 0,3 (моль) * 22,4 (л/моль) = 6,7 (л)
ответ: V(CO2)= 6,7 (л).
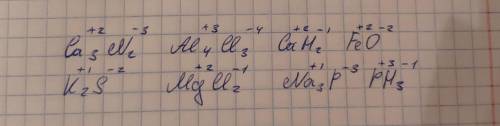
Все тела живой и неживой природы, несмотря на их разнообразие, состоят из мельчайших частиц — атомов. Первым, кто высказал предположение об этом, считается древнегреческий философ Демокрит. Именно он назвал атомом мельчайшую неделимую частицу образующую вещество (атом в переводе с др.греч «неделимый»). Лишь в конце XIX в. были сделаны открытия, показавшие сложность строения атома, что атомы разлагаются на более мелкие элементарные частицы и таким образом «атомами» в Демокритовском смысле не являются. Тем не менее, термин используется и теперь в современной химии и физике, несмотря на несоответствие его этимологии современным представлениям о строении атома.строение атома исторя развития
Первые представления об атоме
Демокрит считал, что если разделить, например, яблоко на две половины, затем одну из них еще на две части, и продолжать деление таким образом до тех пор пока результат деления перестанет быть яблоком, то мельчайшая частица которая все еще сохраняет свойство яблока является атомом яблока (т.е. неделимой частью яблока). Он утверждал, что атомы существуют вечно; они настолько малы, что их размеры не поддаются измерению; все атомы одинаковы, но они различаются внешне (атомы воды, например, гладкие, они перекатываться, и поэтому жидкости свойственна текучесть; атомы железа имеют зубчики, которыми они зацепляются друг за друга, что придает железу свойства твердого тела). Представления Демокрита были умозрительными.