1. А) N2 + 3Н2 = 2NН3 - соединения
Б) 3Mg + 2H3РО4 = Mg3(РО4)2 +3 H2↑ - замещения
В) 2Al(OH)3 = Al2O3 + 3H2O - разложения
Г) 2Cu2O = 4Cu + O2↑ - разложения
2. Na2CO3 + 2HCl = 2NaCl + H2O + CO2 - ионного обмена.
признаки: выделение воды и газа, индикатор показывает нейтральный pH (в первом растворе (Na2CO3) изначально показывалась щелочная среда, во втором (HCl) - кислая)
2 + + 2+2=2+2+ H2O + CO2
+ 2=H2O + CO2
3. 2Mg+O2=2MgO
Магний+кислород=оксид магния
MgO+2HCl=MgCl2+H2O
оксид магния+соляная кислота=хлорид магния +вода
MgCl2+2KOH=Mg(OH)2+2KCl
хлорид магния+гидроксид калия= гидроксид магния + хлорид калия
4. 2 + 6 =2 +3
--3e-> 3 2 окислитель
2-+2e-> 2 3 восстановитель
Объяснение:
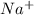

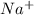
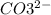

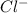
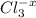


вар.1) 17г 22,2г хг
2AgNO3 + CaCl2 = 2AgCl + Ca(NO3)2
v=2моль v=1моль v=2моль
М=170г/моль М=111г/моль М=143,5г/моль
m=340г m=111г m=287г
найдем избыток и недостаток
17/340 < 22,2/111
AgNO3-недостаток,расчет ведем по недостатку
v(AgNO3)=17г/(170г/моль)=0,1моль
v(AgNO3)=v(AgCl)=0,1моль
m(AgCl)=M*v=143,5г/моль*0,1моль=14,35г
ответ:14,35г хлорида серебра
вар2.) 26,1г 4,5г хг
Ba(NO3)2 + H2SO4 = BaSO4 + 2HNO3
v=1моль v=1моль v=1моль
М=261г/моль М=98г/моль М=233г/моль
m=261г m=98г m=233г
26,1/261 >4,5/98
H2SO4-недостаток
v(H2SO4)=4,5г/(98г/моль)=0,046моль
v(BasO4)=v(H2SO4)=0,046моль
m(BaSO4)=0,046моль*233г/моль=10,7г
ответ:10,7г сульфата бария
вар3) 50г 20г хг
CuSO4 + 2NaOH = Cu(OH)2 + Na2SO4
v=1моль v=2моль v=1моль
М=160г/моль М=40г/моль М=142г/моль
m=160г m=80г m=142г
50/160 > 20/80
NaOH-недостаток
v(NaOH)=20г/(40г/моль)=0,5моль
v(Na2SO4)=v(NaOH):2=0,5моль:2=0,25моль
m(Na2SO4)=0,25моль*142г/моль=35,5г
ответ:35,5 г сульфата натрия
H₂SeO₄ ( селеновая кислота чем сможете!!
2. Установите качественный состав кислоты, общее количество атомов.
3. Подсчитайте относительную молекулярную массу (Mr).
Mr (H₂SeO₄ )= 1*2 + 78,96 + 16*4 = 2 + 78,96 + 64 = 144,96 г/моль
4. Вычислите массовую долю каждого элемента, входящего в кислоту.
W (H₂) = 2 / 144,96 *100 % = 1,38 %
W (Se) =78,96 / 144,96 * 100 % =54,47 %
W (O₄) = 64 / 144,96 * 100 % = 44,15 %
проверка:
W (H₂) +W (Se) + W (O₄) = 1,38 % + 54,47 % + 44,15 % = 100 %
5. Классифицируйте данное соединение:
H₂SeO₄ - селеновая кислота: двуосновная, кислородосодержащая, сильная
а) по наличию атомов кислорода;
содержит 4 атома кислорода
б) по количеству атомов водорода;
содержит 2 атома водорода
в) по растворимости в воде .
хорошо растворима в воде
6. Вычислите степень окисления всех элементов, входящих в кислоту.
H₂⁺¹Se⁺⁶O₄ ⁻²
7. Определите заряд кислотного остатка.
H₂⁺¹(SeO₄ )⁻²
8. Установите соответствующий кислоте оксид (если сможете).
SeO₃ - оксид селена (VI)
9. Вычислите массу 0,5 моль вашей кислоты
m(H₂SeO₄) = M * n
m(H₂SeO₄) = 144. 96 * 0.5 моль = 72,48 г