Задание 1 ( ).
Заполните таблицу:
Свойства
Азотная кислота
Соли азотной кислоты
Химическая формула вещества
Тип химической связи
Агрегатное состояние при н. у.
Цвет
Растворимость в воде
Окислительно-восстановительные свойства
Применение
Задание 2 ( ).
Требования к оформлению уравнений реакций
Даны вещества: хлорид натрия, карбонат натрия, гидроксид калия, оксид магния, гидроксид цинка, серебро. С какими из них взаимодействует концентрированная азотная кислота? Составьте уравнения возможных реакций.
Молекулярные уравнения
Сокращённые ионные уравнения
Составьте электронный баланс к уравнению реакции азотной кислоты с простым веществом. Укажите окислитель и восстановитель, процессы окисления и восстановления. Расставьте коэффициенты методом электронного баланса.
Задание 3 ( ).
Требования к оформлению уравнений реакций
Напишите уравнения термического разложения нитратов.
Название соли
Уравнение реакции разложения соли
Нитрат натрия
Нитрат магния
Нитрат ртути
Пошаговое объяснение:
20
Пошаговое объяснение:
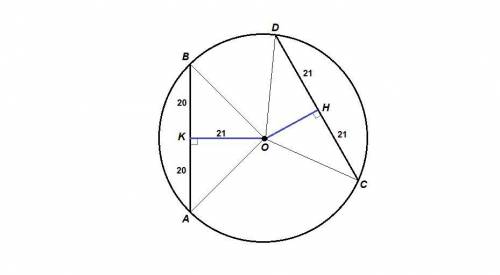
Соединим центр окружности с концами хорд.
ОА = ОВ = ОС = OD как радиусы.
Проведем ОК⊥АВ и и OH⊥CD,
ОК = 21 - расстояние от центра до АВ,
ОН - искомое расстояние от центра до CD.
ΔОАВ равнобедренный, значит ОК - высота и медиана. ⇒
АК = КВ = 1/2АВ = 1/2 · 40 = 20
Из прямоугольного треугольника АКО по теореме Пифагора:
АО = √(АК² + КО²) = √(20² + 21²) = √(400 + 441) = √841 = 29
СО = АО = 29
ΔCOD равнобедренный, значит OН - высота и медиана, ⇒
СН = HD = 1/2CD = 1/2 · 42 = 21
Из прямоугольного треугольника СОН по теореме Пифагора:
OH = √(CO² - CH²) = √(29² - 21²) = √(841 - 441) = √400 = 20
80/20=4 - купили 4 отвертки и 4 ножовки