уравнение Менделеева-Клапейрона

из этого же уравнения выводятся несколько других
Закон Шарля (описывает изохорный процесс)
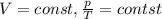
Закон Гей-Люссака (описывает изобарный процесс)
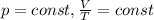
и Закон Бойля-Мариотта (описывает изотермический процесс)

их названия, конечно, знать вовсе не обезательно, и воводятся они из первого уравнения довольно легко.
также внутрянняя энергия идеального газа
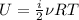
где i - количество степеней свободы (для одноатомного газа 3, для двухатомного 5)
работа идеального газа
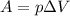
Также первый закон термодинамики
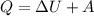
Q - кол-во теплоты, U - внутр. энергия, A - соверш. работа.
p = 760 мм. рт. ст. 760·133,3 ≈ 1·10⁵ Па
<Vкв> = 400 м/с
ρ - ?
1)
Запишем формулу среднеквадратичной скорости:
<Vкв> = √ ( 3·R·T/M)
Возведем ее в квадрат:
<Vкв>² =3·R·T/M
Отсюда:
R·T = M·<Vкв>²/3 (1)
2)
Запишем уравнение Менделеева-Клапейрона:
p·V = m·R·T / M
Разделим на объем:
p = (m/V)·R·T / M
Учтем, что плотность ρ = m/V
p = ρ·R·T / M
Отсюда:
R·T = p·M / ρ (2)
3)
Приравняем (1) и (2):
M·<Vкв>²/3 = p·M / ρ
Отсюда:
ρ = 3·p·/ <Vкв>² (M - сократили).
Подставляем:
ρ = 3·p·/ <Vкв>² = 3·1·10⁵ / 400² ≈ 1, 9 кг/м³