ОбъяснЗадача 3.
В объемом V = 7,5 л при Т = 300 К находится смесь идеальных газов: ν1 = 0,1 моля О2, ν2 = 0,2 моля N2, ν3 = 0,3 моля СО2. Найти: давление в смеси и среднюю молекулярную массу данной смеси .
Дано: V = 7,5 л = 7,5·10–3 м3, Т = 300 К, ν1 = 0,1 моля О2, ν2 = 0,2 моля N2, ν3 = 0,3 моля СО2.
Решение. По определению в идеальном газе молекулы не взаимодействуют между собой, поэтому для смеси идеальных газов уравнение состояния (3.1) можно записать в виде:
,
откуда:
.
Для нахождения средней молярной массы смеси воспользуемся определением числа молей газа ν = m/M, где m и М – масса и молярная масса газа, соответственно.
Тогда:
. (1)
Введя среднюю молярную массу и массу смеси , получим:
pV = mRT/. (2)
Из сравнения (1) и (2) следует, что:
.
Заменяя mi = νiMi (i = 1, 2, 3) и , получим:
.ение:
Сначала определим среднюю квадратичную погрешность измерения мощности:
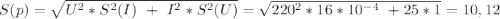
Тогда доверительный интервал измерения Р при указанной доверительной вероятности и коэффициентом Стьюдента t = 2,77 равен:
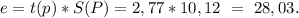
Тогда результат измерения мощности можно записать в виде:
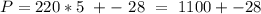
ответ: 1100 +- 28 Вт.
P.S. Не понял начало задания про систематическую погрешность...Это другая какая-то задача? Или часть всего задания? Я делал без учета систематической погрешности измерения напряжения, ориентируясь только на данные второй части задания. Если нужно учесть систематическую погрешность, то в формулу для вычисления ср. квадр. погрешности мощности я бы вместо 220 подставил 222 и погрешность будет безусловно выше...