6 г х моль
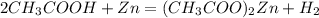
120 г 1 моль
1. Знайдемо чисту массу етанової кислоти у розчині:
m(CH3COOH)=m(розчину)*w(CH3COOH)=50*0,12=6 г
2. Підставивши цю масу у рівняння,розрахуємо кількість речовини водню:
при взаємодії 120 г кислоти виділяється 1 моль водню, а
при -- // -- 6 г____________________х г, звідки
х=6*1/120=0,05 моль
3. А тепер з формули по визначенню кількості речовини, знайдемо:
а) m(H2)=M(H2)*v(H2)=2*0,05=0,1 г
б) V(H2)=Vm(H2)*v(H2)=22,4*0,05=1,12 л
6 г х моль
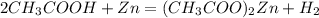
120 г 1 моль
1. Знайдемо чисту массу етанової кислоти у розчині:
m(CH3COOH)=m(розчину)*w(CH3COOH)=50*0,12=6 г
2. Підставивши цю масу у рівняння,розрахуємо кількість речовини водню:
при взаємодії 120 г кислоти виділяється 1 моль водню, а
при -- // -- 6 г____________________х г, звідки
х=6*1/120=0,05 моль
3. А тепер з формули по визначенню кількості речовини, знайдемо:
а) m(H2)=M(H2)*v(H2)=2*0,05=0,1 г
б) V(H2)=Vm(H2)*v(H2)=22,4*0,05=1,12 л
Объяснение:
КOH + HNO3=КNO3+H2O
Запишем молярную массу гидроксида натрия и азотной кислоты:
Mr(КOH)=39+1+16=56 г/моль
Mr(HNO3)=1+14+3*16=63 г/моль
Вычислим количество вещества растворенного КOH и HNO3 :
n(КOH)=m(КOH)/Mr(КOH)=6/56=0,1071 моль
n(HNO3)=m(HNO3)/Mr(HNO3)=6/63=0,0952 моль
Как видим, в растворе избыток щелочи, она не полностью прореагирует, среда будет щелочной. Окраска индикатора зависит от того, какой взяли индикатор. Фенолфталеин, например, в щелочной среде будет малиновым.