1. Поваренная соль ( кухонная соль - NaCl ) в отличии от песка ( SiO2 ) растворима в воде, песок выпадет в осадок, раствор соли, отфильтровать, воду из раствора выпарить
2. Воду можно выпарить от соли
3 -
4.
Действие магнитом ( если в смеси есть железо);
Фильтрование ( растворимая от нерастворимой, например: воду или раствор соли в воде от мела );
Отстаивание ( если компоненты не смешиваются, например: вода и масло );
Выпаривание и кристаллизация ( растворимую в воде вещество, например: кухонная соль в воде )
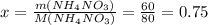 моль
моль![y= \frac{m[Me(NO_3)_2]}{M[Me(NO_3)_2]}= \frac{40}{(Mr+124)}](/tpl/images/0580/1169/cc224.png) моль
моль![w(N)= \frac{m_1(N)+m_2(N)}{m(NH_4NO_3)+m[Me(NO_3)_2]}](/tpl/images/0580/1169/63d03.png)
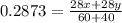
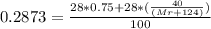
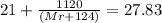
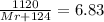
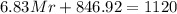
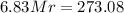
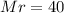 г/моль
г/моль
объем соляной кислоты: Vр-ра(НС1) = 300 мл;
массовая доля НС1 в соляной кислоте: типовые задачи по химии(НС1) = 4% ;
плотность соляной кислоты: рр-ра(НС1) = 1,02 г/мл.
Найти: массу Mg3N2.
Решение:
В условии задачи описано несколько последовательных химических реакций.
Мg3N2 + 6Н2O = ЗМg(ОН)2 + 2NH3 ( 1 )
Оба продукта первой реакции будут взаимодействовать с соляной кислотой с образованием солей.
Мg(ОН)2 + 2НС1 = МgС12 + 2Н2О (2)
NH3 + НС1 - NH4С1 (3)
Решение данной задачи необходимо вести с составлением математического уравнения. Схематично алгоритм можно представить таким образом:
массовая доля, тестовые задачи по химии
1. Обозначим количество вещества1 исходного Mg3N2 величиной «а»: n(Mg3N2) = а моль.
Используя величину «а» как известную, по первому химическому уравнению определяем количество вещества каждого из продуктов:
массовая доля, тестовые задачи по химии
2. По второй химической реакции определяем количество вещества НС1, которое расходуется на солеобразование с (3а) моль Mg(OH)2.
массовая доля, тестовые задачи по химии
3. По третьей химической реакции определяем количество вещества НС1, которое расходуется на солеобразование с (2а) моль МН3.
массовая доля, тестовые задачи по химии
4. Определяем общее количество НС1, которое расходовалось в реакциях №2 и №3 по результатам расчета в предыдущих двух действиях.
n(HCl)общее = n(HCl)в р-ции№2 + n(НС1)в р-ции№3 = 6а + 2а = (8а) моль.
5. Определяем количество вещества НС1, которое содержалось в 300 мл 4% -ного раствора (по данным условия):
массовая доля, тестовые задачи по химии
6. Составляем математическое уравнение. Для этого приравниваем количество вещества НС1, определенное путем расчета по химическим уравнениям (из 4 действия), и значение, найденное в 5 действии:
8а = 0,335.
Решая это математическое уравнение, находим значение величины «а»:
а = 0,042 моль.
Величиной «а», мы обозначали количество вещества исходного Мg3N2: n(Мg3N2) = 0,042 моль.
7. Определяем массу исходного вещества:
m(Мg3N2) = n(Мg3N2) . M(Мg3N2) = 0,042 . 100 = 4,2 г.
ответ: m(Мg3N2) = 4,2 г.
Комментарии:
1Величиной «а» можно было обозначить и массу исходного вещества. В этом случае в расчетах фигурировали бы более сложные значения, и возросла вероятность арифметической ошибки.