Кислоты-это електролиты,которые в водных растворах и розплавах диссоциируют на катионы Водорода и анионы кислотных остатков.За наличием атомов Кислорода их делят на кислородсодержащие(H2SO4,HNO3) и безкислородные(HCl,H2S).По количеству атомов Водорода кислоты бывают одноосновные(HNO3,HCl), двуосновные(H2CO3,H2S) и триосновные(H3PO4).По степени диссоциации кислоты делят на сильные(HCl), средней силы(H3PO4) и слабые(H2CO3)
Химические свойства:
1.Диссоциация
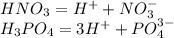
2.Взаимодействуют с основными оксидами:
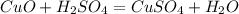
3.С основаниями(щелочами и нерастворимыми):
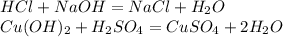
4. С амфотерными оксидами и гидроксидами:
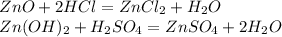
5. С солями более слабых кислот:
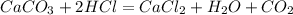
6. С металлами:

1) окисление этилбензола перманганатом калия (например в кислой среде) приводит к получению бензойной к-ты:
5C6H5-CH2-CH3 + 12KMnO4 + 18H2SO4 = 5C6H5-COOH (бензойная к-та) + 5CO2 + 28H2O + 6K2SO4 + 12MnSO4;
2) C6H5-COOH + NaOH = C6H5-COONa (бензоат натрия) + H2O;
3) в зависимости от мольного соот-ия C6H5-COONa и H2 может получится бензальдегид C6H5-CHO и бензиловый спирт C6H5-CH2-OH:
C6H5-COONa + H2 (+T, Ni) = C6H5-CHO + NaOH, далее:
C6H5-COONa + 2H2 (+T, Ni) = C6H5-CH2-OH + NaOH.