1. Распределите следующие вещества соответственно типам химической связи:
H2O, Br2, CO2, H2S, NaF, H2, Cu, CS2, MgO, C, KCl, NH3, P2O5, MgS, F2, NaCl, Al2O3
2. Запишите механизм образования химической связи в веществах Cl2, NH3, NaF
3. Определите тип кристаллической решетки
NH3, P2O5, MgS, F2, NaCl
4. Дайте определение понятий «степень окисления», «окислительно-восстановительная реакция», «окисление», «восстановление».
5. В следующих уравнениях определите окислитель и восстановитель, расставьте коэффициенты
P + Cl2 =PCl3
Al + O2 = Al2O3
6. Домашнее задание: § 36-43 (повторить)
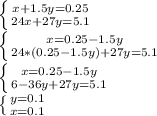 . Зная количество вещества каждого металла, можем найти массу этих металлов: m (Mg)=2.4 грамм, а m (Al)=2.7 грамм.
. Зная количество вещества каждого металла, можем найти массу этих металлов: m (Mg)=2.4 грамм, а m (Al)=2.7 грамм.
Найдем количество вещества (H2O) по формуле n=V/Vm, где Vm=22.4 литр/моль. n (H2O)=180/22.4=8 моль. По уравнению реакции n (O2)=8/2=4 моль. Найдем объем кислорода по формуле V=n*Vm. V (O2)=4*22.4=89.6 литров.
2) Относительная плотность сероводорода по воздуху будет равна частному молекулярной массы сероводорода и воздуха. Относительная плотность (H2S)=34/29=1.17.
3) Сначала найдем количество вещества фтора по формуле n=m/M. n (F2)=38/38=1 моль. Найдем объем фтора по формуле V=n*Vm, где Vm=22.4 литр/моль. V (F2)=1*22.4=22.4 литра.