х г 66,6 л
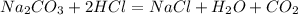
106 г 22,4 л
1. Найдем массу прореагировавшего карбоната:
при взаимодействии 106 карбоната выделится 22,4 л, а
при -- // -- х г___________________66,6 л, откуда
х=106*66,6/22,4=315 г
2. Найдем массу раствора карбоната натрия:
если 1000 л содержит 1102 кг, то
4 л__________у кг, откуда у=4*1102/1000=4,408 кг или 4 408 г
3. Теперь отнеся массу карбоната к массе всего раствора,определим массовую долю карбоната в нем:
m(Na2CO3)=m(NaCO3)/m(раствора)=315/4408=0,07 или 7%
ответ:
объяснение:
ацетилен из метана можно получить двумя способами, оба из которых подходят к указанной схеме ch4 -> c2h2. во-первых, если проводить термоокислительный крекинг метана, то в качестве одного из многочисленных продуктов реакции образуется ацетилен. уравнение реакции имеет вид:
\[6ch_4 + 4o_2 \rightarrow c_2h_2 + 8h_2 + 3co + co_2 +
во-вторых, одним из наиболее популярных методов получения ацетилена из метана является пиролиз последнего, проводимый при температуре 1600^0 c. уравнение реакции имеет вид:
\[2ch_4 \rightarrow c_2h_2 +
теперь переходим к решению . первоначально рассчитаем количество молей метана, вступившего в реакцию пиролиза (m(ch_4) = 16 g/mole):
\[n \rightarrow m \div m; \]
\[n (ch_4) \rightarrow m(ch_4) \div m(ch_4) \rightarrow 80 \div 16 \rightarrow 5
согласно уравнению реакции n(ch_4) : n(c_2h_2) = 2: 1, значит n(c_2h_2) = n(ch_4) \div 2 = 5 \div 2 = 2,5 mole. тогда масса ацетилена будет равна (молярная масса – 26 g/mole):
\[ m (c_2h_2) \rightarrow n(c_2h_2) \times m(c_2h_2) \rightarrow 2,5 \times 26 \rightarrow 65