Объяснение:
В промышленности и с/х -ве применяют два вида фосфатов аммония.
NH4H2PO4 - дигидрофосфат аммония (аммофос)
(NH4)2HPO4 - гидрофосфат аммония (диаммофос)
Оба вещества растворимы в воде.
Доказать наличие иона аммония NH4+ в составе вещества легко.
Достаточно к раствору вещества добавить крепкий раствор щелочи и нагреть или несколько раз встряхнуть пробирку. Появляется характерный запах аммиака.
NH4+ + NaOH = Na+ + NH4OH
Гидроксид аммония, а точнее гидрат аммиака NH3 · H2O вещество не стойкое и разлагается на аммиак и воду.
Реактивом на фосфат-ион РО4(3-) служит раствор нитрата серебра:
PO4(3-) + 3AgNO3 = Ag3PO4 ↓ + 3NO3(-)
желтый осадок
1. 1) Щёлочи:
Щёлочь + кислота = соль + вода
NaOH + HCl → NaCl + H₂O
Na⁺ + OH⁻ + H⁺ + Cl⁻ → Na⁺ + Cl⁻ + H₂O
H⁺ + OH⁻ → H₂O
Щелочь + оксид металла = соль + вода, ЕСЛИ ОКСИД МЕТАЛЛА - АМФОТЕРНЫЙ
2KOH + Al₂O₃ → 2KAlO₂ + H₂O
2K⁺ + 2OH⁻ + Al₂O₃ → 2K⁺ + 2AlO₂⁻ + H₂O
Al₂O₃ + 2OH⁻ → 2AlO₂⁻ + H₂O
Щелочь + соль = основание + соль
2LiOH + Zn(NO₃)₂ → 2LiNO₃ + Zn(OH)↓ (реакция возможна, если образуется осадок)
2Li⁺ + 2OH⁻ + Zn²⁺ + 2NO₃⁻ → 2Li⁺ + 2NO₃⁻ + Zn(OH)₂↓
Zn²⁺ + 2OH⁻ → Zn(OH)₂↓
2) Нерастворимое основание:
Нерастворимое основание + кислота = соль + вода
Cu(OH)₂ + H₂SO₄ → CuSO₄ + 2H₂O
Cu(OH)₂ + 2H⁺ + SO₄²⁻ → Cu²⁺ + SO₄²⁻ + 2H₂O
Cu(OH)₂ + 2H⁺ → Cu²⁺ + 2H₂O
Нерастворимое основание → t° → оксид металла + вода
Mn(OH)₂ → MnO + H₂O
2. Как характеризовать гидроксид бария по таблице 11 - не ясно. Напишу все, что знаю по нему:
Гидроксид бария - Ba(OH)₂: растворимое основание, проявляет оснОвные свойства. Взаимодействует с кислотами с образованием соли и воды:
Ba(OH)₂ + 2HNO₃ → Ba(NO₃)₂ + 2H₂O
Взаимодействует с кислотными оксидами с образованием солей и воды:
Ba(OH)₂ + SO₃ → BaSO₄↓ + H₂O
Взаимодействует с амфотерными оксидами и гидроксидами:
Ba(OH)₂ + 2Al(OH)₃ → Ba[Al(OH)₄]₂
Ba(OH)₂ + Al₂O₃ → Ba(AlO₂)₂ + H₂O
И взаимодействует с солями (если образуется осадок)
Ba(OH)₂ + Na₂SO₄ → BaSO₄↓ + NaOH
Решение 3 во вложении ↓
НО никакого осадка там не образуется... Na₂CO₃ - растворим в воде, можно убедится по таблице растворимости
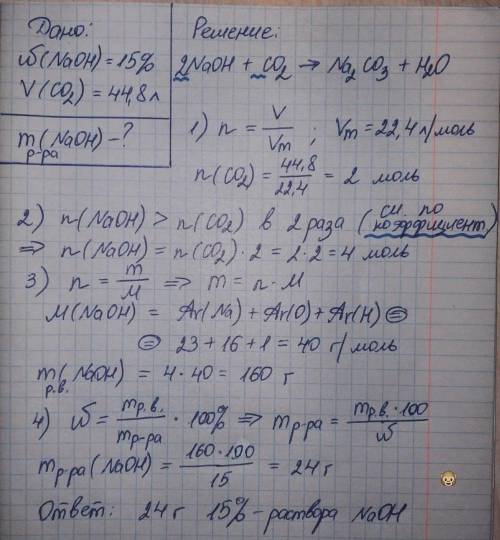
Объяснение:
Ca + 2C = CaC2
CaC2 +2HCl = CaCl2 +C2H2
C2H2 + HCl = CH2=CHCl
CH2=CHCl + H2 - (Pt) -> C2H5Cl
C2H5Cl + NaOH -(H2O) -> C2H4 + NaCl + H2O