Дисперстные системы дисперсные системы - системы, представляющие собой механическую смесь частиц дисперсной фазы со средой-носителем. такие системы являются широко распространенным объектом в природе и повседневной деятельности человека. образование облаков и выпадение осадков, формирование аэрозольной компоненты земной атмосферы, эволюция допланетного роя и частиц межзвездной пыли, миграция дефектов в твердых телах, двухфазные течения в и промышленных установках, перенос в атмосфере различного рода промышленных и радиоактивных загрязнений - все это далеко не полный круг явлений, в которых решающую роль играют процессы, происходящие с дисперсными системами. обычно дисперсные системы подразделяют, исходя из агрегатного состояния частиц дисперсной фазы и среды-носителя. ряд дисперсных систем получил отдельные названия: •аэрозоли (взвесь твердых или жидких частиц в газовой среде, обычно в воздухе) ; •эмульсии (жидкие частицы, обычно стабилизированные защитными оболочками, в жидкой среде) •коллоиды (взвесь твердых частиц в жидкой среде) ; •астрозоли (твердые или жидкие частицы в вакууме) кроме того, существуют дисперсные системы без устоявшихся названий: ансамбли газовых пузырьков в твердом теле или жидкости, ансамбли жидких капель в твердом теле и т. д. дисперсные системы многими необычными свойствами, которые требуют отдельного изучения и сказываются на практике. так, отдельно взятая молекула вещества в газовом состоянии имеет одни свойства, в сплошном состоянии – другие свойства, а в состоянии аэрозоли (дисперсная фаза) уже совсем другие свойства, которые являются плавным переходом от газообразной к твёрдой фазе. можно назвать своеобразную газодинамику, обусловленную различным движением среды-носителя и частиц дисперсной фазы; необычные оптические свойства, вызванные сравнимостью размеров частиц с длинами волн света и влиянием формы частиц; повышенную способность к взаимодействиям, вызванную чрезвычайно развитой поверхностью частиц.
здесь используется правило Вант -Гоффа
хотела с текстовым редактором ...не получилось
попробуем без него
Vt2
----- =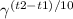
Vt1
320/80 =
8 =