ответ: В 2-х молях углекислого газа содержится 1,204*10²⁴ молекул и 3,612*10²⁴ атомов
Объяснение:
В 2 моль углекислого газа СО2 содержится 2 моль молекул и 6 моль атомов (2 моль атомов углерода и 4 моль атомов кислорода).
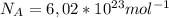
По формуле 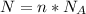 найдем количество молекул и атомов, где n - количество вещества (атомов);
найдем количество молекул и атомов, где n - количество вещества (атомов); 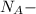 постоянная Авогадро.
постоянная Авогадро.
N = 2 моль*6,02*10²³ молекул/моль = 1,204*10²⁴ молекул
N = 6 моль*6,02*10²³ атомов/моль = 3,612*10²⁴ атомов
ответ: В 2-х молях углекислого газа содержится 1,204*10²⁴ молекул и 3,612*10²⁴ атомов
Sn(NO₃)₂:
Sn(OH)₂ ← Sn(NO₃)₂ → HNO₃
Sn(OH)₂ - слабое двухкислотное основание [OH⁻] => [OH⁻]<[H⁺]
HNO₃ - сильная одноосновная кислота [H⁺] pH<7
Первая ступень (стадия) гидролиза:
Sn(NO₃)₂ + HOH ⇄ SnOHNO₃ + HNO₃ - молекулярное уравнение
Sn²⁺ + 2NO₃⁻ + HOH ⇄ SnOH⁺ + NO₃⁻ + H⁺ + NO₃⁻ - полное ионное уравнение
Sn²⁺ + HOH ⇄ SnOH⁺ + H⁺ - сокращенное (краткое) ионное уравнение
Вторая ступень (стадия) гидролиза:
SnOHNO₃ + HOH ⇄ Sn(OH)₂↓ + HNO₃
SnOH⁺ + NO₃⁻ + HOH ⇄ Sn(OH)₂↓ + H⁺ + NO₃⁻ - полное ионное уравнение
SnOH⁺ + HOH ⇄ Sn(OH)₂↓ + H⁺ - сокращенное (краткое) ионное уравнение
В результате гидролиза образовались ионы водорода (H⁺), поэтому раствор имеет кислую среду (pH < 7).
Rb₂S:
RbOH ← Rb₂S → H₂S
RbOH - сильное однокислотное основание [OH⁻] => [OH⁻]>[H⁺]
H₂S - слабая одноосновная кислота [H⁺] pH>7
Первая стадия гидролиза :
Rb₂S + H₂O ⇄ RbOH + RbHS - молекулярное уравнение
2Rb⁺ + S²⁻ + H₂O ⇄ Rb⁺ + OH⁻ + Rb⁺ + HS⁻ - полное ионное уравнение
S²⁻ + H₂O ⇄ HS⁻ + OH⁻ - сокращенное (краткое) ионное уравнение
Вторая стадия гидролиза :
RbHS + H₂O ⇄ RbOH + H₂S↑ - молекулярное уравнение
Rb⁺ + HS⁻ + H₂O ⇄ Rb⁺ + OH⁻ + H₂S↑ - полное ионное уравнение
HS⁻ + H₂O ⇄ OH⁻ + H₂S↑ - сокращенное (краткое) ионное уравнение
Т.к. в результате гидролиза образовались гидроксид-ионы (OH⁻), то раствор будет имеет щелочную среду (pH > 7).