СН4 = С + 2Н2
Составляеи пропорцию и находим m теорет. (С):
200000 г СН4 - х г С
16 г/моль СН4 - 12 г/моль С
х г = 150000
m практ. = 150000 * 0,9 = 135000 г
ответ: 135000 г
5,4 г 7,3 г,х г у л
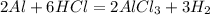
54 г 219 г 67,2 л
1. Сначала найдем чистую массу кислоты в растворе:
m(HCl)=m(раствора)*w(HCl)=73*0,1=7,3 г
2. Теперь определим,какое из исходных веществ прореагирует полностью, приняв массу,например,кислоты за Х:
для полного взаимодействия 54 г алюминия потребуется 219 г кислоты, а
для -- // -- 5,4 г____________________х г, откуда
х=5,4*219/54=21,9 г
3. Но так как по условиям дано всего 7,3 г,значит алюминий останется в избытке,поэтому расчет объема водорода ведем по массе кислоты:
при взаимодействии 219 г кислоты выделяется 67,2 л водорода, а
при -- // -- 7,3 г___________________у л, откуда
у=7,3*67,2/219=2,24 л
1 задание.
1. ЗАпишем уравнение реакции: 3Al+2H2SO4 = Al3(SO4)2+2H2
Рассчитаем количества вещества:
n(Al)=5.4/27=0.2моль
m(H2SO4)=80*0.2=16гр, n(H2SO4)=16/98=0,1632моль
Серная кислота в недостатке, по ней и считаем.
n(H2)=n(H2SO4)=0,1632 моль.
V(H2)=0.1632*22.4=3.657л
m(H2)=0.1632*2=0.3264гр.
2 задание.
1. ЗАпишем уравнение реакции: Zn+2HCl = ZnCl2+H2
2. Рассчитаем количество вещества:
n(Zn)=26/65=0.4моль
m(HCl)=300*0.073=21.9гр
n(HCl)=21.9/36.5=0.6моль
Цинк в недостатке, по нему и считаем
n(Zn)=n(H2)=0.4моль
V(H2)=0,4*22,4=8,96моль
m(H2)=0.4*2=0.8гр
Метан СН4 содержит 12/(12 + 4) = 0,75, или 75% по массе углерода С.
200 кг метана содержат 200*0,75 = 150 кг углерода.
С учетом выхода в 90% масса сажи составит 150*0,9 = 135 кг, или 135 000 граммов.