1) Реакции:
С2Н5ОН + [O] = СН3СНО + Н2О
2СН3СНО + О2 = 2СН3СООН
СН3СООН + СН3ОН = СН3СООСН3 + Н2О
2)Решение:
С+O2=CO2
расчитаем количество вещества углерода
n(C)=n(CO2) по реакции
n(CO2)=m/M=0.1/44=0.002 моль
n(C)=n(CO2)=0.002 моль
расчитаем массу углерода в стальной проволоке
m(C)=M*n=12*0.002=0.024 г
расчитаем массовую долю углерода
w(C)=m(C)/mпроволоки*100%=0,024/5*100=0,48%
ответ: 0,48 %.
3)C2H5OHдегидратация в присутствии H2SO4(конц)=С2H4+H2O
C2H4 +HCl---C2H5HCl(реакция присоединения при температуре и давлении)
2С2H5HCl+2NaC4H10=2NaCl(реакция вьюрца)
4)Решение:
Водород выделяется только при взаимодействии кальция с водой
Ca+2H2O=Ca(OH)2+H2
1. Найдем массу кальция по выделившемуся водороду(н.у.) пропорцией:
x - 40 г
2.8 л - 22.4 л »»» x=2,8*40/22.4=5 г. (Са)
2. Рассчитаем массовую долю кальция:
W(Ca)=m(Ca)/m(смеси)=5/7,8=0,641 (или 64,1%)
ответ: 64,1%.
+6 -1
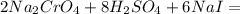
0 +3
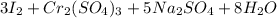
+6 +3
Cr + 6e = Cr |1| окислитель(восстановление)
-1 0
2I - 2e = I2 |3| восстановитель(окисление)
+6 +2
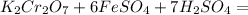
+3 +3
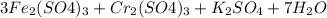
+6 +3
Cr + 6e = Cr |1| окислитель(восстановление)
+2 +3
Fe - 2e = Fe |3| восстановитель(окисление)
+5 +3 +6 -1
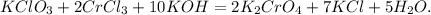
+5 -1
Cl + 6e = Cl |1| окислитель(восстановление)
+3 +6
Cr - 3e = Cr |2| восстановитель(окисление)
FeSO4 = Fe(2+) + SO4(2-)
Na3PO4 = 3Na(+) + PO4(3-)
RbOH = Rb(+1) + OH(-)
2) ZnCl2 + Na2S=ZnS + 2NaCl
2NaOH + H2SO4=Na2SO4 + H2O
Cu(OH)Cl + NaOH = Cu(OH)2 + NaCl
NaHCO3 + HCl=NaCl + H2CO3
CH3COOK + HCl = CH3COOH + KCl
Pb(NO3)2 + 2KI = PbI2 + 2KNO3
3) 2I(-) -2e = I2(0) |4
S(+6) +8e = S(-2) |1
8KI + 9H2SO4 = 8KHSO4 + 4I2 + H2S + 4H2O
общую сумму коэффициентов в уравнении 34