Уравнение реакции:
Mg + 2HCl = MgCl₂ + H₂↑
Зная массу кислоты и ее молярную массу (складываем атомные массы водорода и хлора, а эти данные берем из таблицы Менделеева), мы можем найти кол-во вещества кислоты. Итак,
m HCl = 7,3 г
M HCl = 36,5 г/моль
ν HCl = m/M
ν HCl = 7,3 г / 36,5 г/моль = 0,2 моль
По уравнению реакции, соляной кислоты в 2 раза больше, чем соли, значит,
ν MgCl₂ = 0,2 моль / 2 = 0,1 моль
Зная кол-во вещества соли и её молярную массу, находим массу:
m = M*ν
m MgCl₂ = 95 г/моль * 0,1 моль = 9,5 г.
ответ: 9,5 г.
Нет.
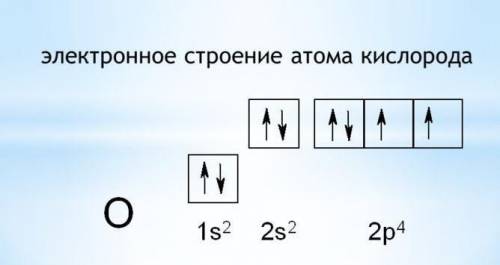
У Кислорода на внешнем уровне(2 уровень), в подуровне р-, два электрона без пары, за счёт них образуются стабильные две связи — валентность II всегда.
У Серы есть ещё и третий уровень, в котором есть s-, p- и d- подуровни. Поэтому у серы больше валентностей. В возбуждённом состоянии сера может проявлять валентность IV и VI кроме II.
Под n на рисунке подразумевается номер уровня.
16S 1s2 2s2 2p6 3s2 3p4 — валентность II, H2S;
16S* 1s2 2s2 2p6 3s2 3p3 3d1 — валентность IV, SO2;
16S** 1s2 2s2 2p6 3s1 3p3 3d2 — валентность VI, Na2SO4
На рисунке представлен внешний электронный уровень у серы в соединениях, указанных в качестве примеров.
У кислорода валентность II ВСЕГДА. Что в простом веществе O2, что в соединении H2O

вообщето не а 18 во 2 Ты где учишься? Нам просто это же задали схаххахаха