n₁(Li₂O) =0,1моль
Объяснение:
Дано:
m(Li)=1,4г.
----------------------------
n(Li₂O)-?
1. Определим молярную массу лития:
M(Li)=7г./моль
2. Определим количество лития в 1,4г.
n(Li)=m(Li)÷M(Li)=1,4г.÷7г./моль=0,2моль
3. Запишем уравнение реакции:
4Li+O₂=2Li₂O
а) по уравнению реакции количество вещества:
n(Li)=4моль n(Li₂O) =2моль
б) по условию задачи количество вещества:
n₁(Li)=0,2моль n₁(Li₂O) =0,1моль
4. ответ: количество вещества оксида лития образуется при взаимодействии с кислородом 1,4 г лития. 0,1моль
n₁(Li₂O) =0,1моль
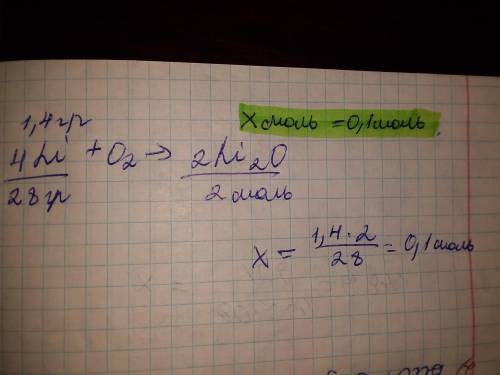
Чтобы нейтрализовать среду, надо добавить вещества с теми ионами, которых не хватает: в кислотную ионы OH- (например NaOH, KOH и т.д.), в щелочную ионы H+ (H2SO4, HCl и др.).
Соответственно, если в задании сказано "составьте реакцию нейтрализации раствора KOH с ", записываешь уравнение реакции:
KOH+HCl = KCl+H2O
Происходит обменная реакция. Если записать в ионном виде, то получится следующее:
K⁺ + OH⁻ + H⁺ + Cl⁻ = K⁺ + Cl⁻ + H2O
(Вода - слабый электролит, в воде на ионы не распадается).
Видно, что щелочной раствор с ионами OH⁻ нейтрализовался ионами H⁺ и в итоге их стало поровну (в данном случае в продуктах реакции их вообще нет).
Если этого достаточно - хорошо, если нет - напишите в комментарии.