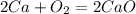
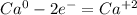 ·2 восстановитель полуреакция окисления
·2 восстановитель полуреакция окисления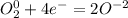 ·1 окислитель полуреакция восстановления
·1 окислитель полуреакция восстановления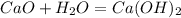
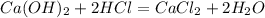
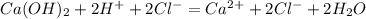
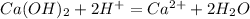
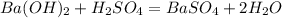
![m[Ba(OH)_2]=](/tpl/images/0276/7725/752a4.png) =50 · 0,18 = 9 г
=50 · 0,18 = 9 г![n[Ba(OH)_2]= \frac{m[Ba(OH)_2]}{M[Ba(OH)_2]} = \frac{9}{171} =0,0526](/tpl/images/0276/7725/43f28.png) моль
моль![n(BaSO_4)=n[Ba(OH)_2]=0,0526](/tpl/images/0276/7725/a4a1c.png) моль
моль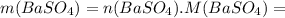 =0,0526 · 233=12,2558 г ≈12,26 г
=0,0526 · 233=12,2558 г ≈12,26 г1) В-во А - оксид углерода (2) CO, металл Б - железо Fe, в-во В - пентакарбонил железа Fe(CO)5, газ Г - оксид углерода CO2, красно-бурое в-во Х - оксид железа (3) Fe2O3, Д - тетракарбонилжелезо Fe(CO)4;
2) а) 5CO + Fe (+T,+P) = Fe(CO)5;
б) 4Fe(CO)5 + 13O2 = 2Fe2O3 + 20CO2;
в) Fe(CO)5 (+T) = Fe + 5CO;
г) Fe(CO)5 (р-р в декане, ультразвук) = Fe + 5CO;
д) Fe(CO)5 (р-р в пентане, ультразвук) = Fe(CO)4 + CO;
е) Fe(CO)4 (+T) = Fe + 4CO;
3) в-во В отн-ся к карбонилам металлов - комплексным соед-м переходных металлов (железа, никеля, кобальта, осмия и т.п.) с монооксидом углерода CO, кот-й явл-ся донором непод-й элек-й пары на атоме углерода, а металл с вак-ми d-орб-ми - акцептором элек-й пары; Co4(CO)12 - черного цвета, V(CO)6 - черного цвета с зелено-синим оттенком, Os2(CO)9 - желтого цвета, Ir2(CO)8 - зеленого цвета;
4) в-во Д также отн-ся к карбонилам металлов (см. 3));
5) светильный газ; его получали при пиролизе каменного угля или нефти; в его составе 50% H2, 34% CH4, 8% оксида углерода CO и др. горючие газы;
6) а) Fe(CO)5 + 3NaOH = Na[Fe(CO)4H] + Na2CO3 + H2O;
б) обр-ся высшие карбонилы: 2Fe(CO)5 (+hv) = Fe2(CO)9 + CO;
в) 2Fe(CO)5 + 3Br2 = 2FeBr3 + 10CO;
г) Fe(CO)5 + 2Na (жидкий NH3) = Na2[Fe(CO)4] + CO.
Объяснение:
Приведенные металлы различаются по химической активности.
Цинк наиболее активен поэтому реагирует с соляной кислотой и другими кислотами-неокислителями.
НСl + Zn = ZnCl2 = H2↑
Аналогично протекает реакция с разбавленной серной кислотой
Н2SO4 + Zn = ZnSO4 + H2↑
с медью и ртутью эти кислоты в разбавленном состоянии не реагируют.
Концентрированная серная кислота вступает в реакцию с медью
Сu + H2SO4 = CuSO4 + SO2↑ + 2 H2O
медь реагирует также с азотной кислотой, как с разбавленной, так и с концентрированной
8HNO3 (разб) + 3Сu = 3 Cu(NO3)2 + 2NO + 4H2O
4HNO3 (конц) + Сu = Cu(NO3)2 + 2NO2 + 2H2O
Ртуть также реагирует с только с кислотами окислителями:
8HNO3 (разб) + 3Нg = 3 Hg(NO3)2 + 2NO + 4H2O
4HNO3 (конц) + Нg = Hg(NO3)2 + 2NO2 + 2H2O
2H2SO4 конц + Hg = НgSO4 + SO2↑ + 2 H2O