Объяснение:
1.
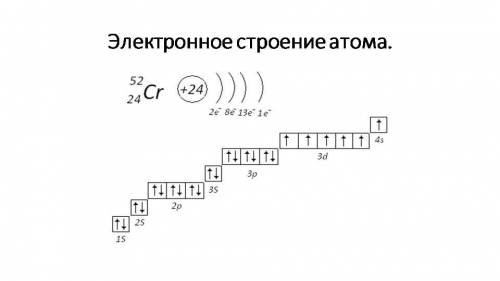
Хром (Cr)
Электронная формула атома: Cr - 1s²2s²2p⁶3s²3p⁶4s¹3d⁵
Электронно графическая формула хрома показана внизу на первом и на втором фотографии↓
2.
а)
серная кислота - H₂SO₄:
В общем виде диссоциацию серной кислоты можно представить в виде:
H₂SO₄⇄ 2H⁺ + SO₄²⁻
1-ая ступень:
H₂SO₄ ⇄ H⁺ + HSO₄⁻
2-ая ступень:
HSO₄⁻ ⇄ H⁺ + SO₄²⁻
Это кислота.
нитрат калия: KNO₃:
В общем виде диссоциацию нитрат калия можно представить в виде: KNO₃ ⇄ K⁺ + NO₃⁻
Это средняя соль (образована сильной щелочью и сильной кислотой).
гидроксид лития: LiOH:
В общем виде диссоциацию гидроксида лития можно представить в виде:
LiOH ⇄ Li⁺ + OH⁻
Это основание.
б)
Na₂SiO₃:
Первая стадия гидролиза :
Na₂SiO₃ + HOH ⇄ NaHSiO₃ + NaOH - молекулярное уравнение
2Na⁺ + SiO₃²⁻ + HOH ⇄ Na⁺ + HSiO₃⁻ + Na⁺ + OH⁻ - полное ионное уравнение
SiO₃²⁻ + HOH ⇄ HSiO₃⁻ + OH⁻ - сокращенное ионное уравнение
Вторая стадия гидролиза :
NaHSiO₃ + H₂O ⇄ H₂SiO₃↓ + NaOH - молекулярное уравнение
Na⁺ + HSiO³⁻ + H₂O ⇄ H₂SiO₃↓ + Na⁺ + OH⁻ - полное ионное уравнение
HSiO₃⁻ + H₂O ⇄ H₂SiO₃↓ + OH⁻ - сокращенное ионное уравнение
Так ка в результате гидролиза образовались гидроксид-ионы (OH⁻), то раствор имеет щелочную среду (pH > 7).
FeS:
Молекулярное уравнение:
FeS + 2H₂O → Fe(OH)₂↓ + H₂S↑
Раствор имеет нейтральную среду.
CuCl₂:
Первая стадия гидролиза :
CuCl₂ + HOH ⇄ CuOHCl + HCl - молекулярное уравнение
Cu²⁺ + 2Cl⁻ + HOH ⇄ CuOH⁺ + Cl⁻ + H⁺ + Cl⁻ - полное ионное уравнение
Cu²⁺ + HOH ⇄ CuOH⁺ + H⁺ - сокращенное ионное уравнение
Вторая стадия гидролиза :
CuOHCl + H₂O ⇄ Cu(OH)₂↓ + HCl - молекулярное уравнение:
CuOH⁺ + Cl⁻ + H₂O ⇄ Cu(OH)₂↓ + H⁺ + Cl⁻ - Полное ионное уравнение:
CuOH⁺ + H₂O ⇄ Cu(OH)₂↓ + H⁺ - сокращенное ионное уравнение
Так как в результате гидролиза образовались ионы водорода (H⁺), то раствор будет иметь кислую среду (pH < 7).
3.
1) С + H₂ → CH₄
2) 2CH₄ + O₂ (t°C, p, кат) → 2CH₃OH
3) CH₃OH + O₂ (t°C, кат) → 2HCOH + H₂O
4) HCHO + Ag₂O (t°) → HCOOH + 2Ag↓
5) HCOOH + C₂H₅OH → HCOOC₂H₅ + H₂O
6) HCOOC₂H₅ + H₂O (NaOH, t°) → C₂H₅OH + HCOOH
Дайте названия веществам (У вас в цепочку все написано то что задали)
4.
пропанол-2: CH₃-CH(CH₃)-OH
пентадиен-1,3: CH₂=CH-CH₂-CH=CH₂
бутановая кислота: CH₃-CH₂-CH₂-COOH
2,4,6 - триметилфенол: C₆H₂(NO₂)₃OH
3-метил-4-этилгексен-1: CH₂=CH-CH(CH₃)-CH(CH₂-CH₃)-CH₂-CH₃
5.
Рассчитайте массу образца сульфата меди (II), если количество вещества составляет 0,6 моль.
Дано:
n(CuSO₄) = 0,6 гр
-------------------------------
Найти:
m(образца CuSO₄) - ?
Мы найдем сначала молекулярную массу сульфата меди (II), а потом мы найдем массу образца сульфата меди (II):
M(CuSO₄) = 64+32+16×4 = 64+32+48 = 160 гр/моль
m(образца CuSO4) = n(CuSO₄)×M(CuSO₄) = 0,6 моль × 160 гр/моль = 96 г р
ответ: m(образца CuSO4) = 96 гр
----------------------------------------------------------------------------------------------
24 мл глицерина растворили в 780 мл воды. Рассчитайте массовую долю данного вещества в растворе.
Дано:
V(HOCH₂-CH(OH)-CH₂OH) = 24 мл
V(H₂O) = 780 мл
------------------------------------------------------------
Найти:
ω(р-р в-ва) -?
1) Сначала найдем массы глицерина и воды, известно что плотность равна 1 гр/мл:
ρ = 1 гр/мл
m(HOCH₂-CH(OH)-CH₂OH) = V(HOCH₂-CH(OH)-CH₂OH)×ρ = 24 мл × 1 гр/мл = 24 гр
m(H₂O) = V(H₂O)×ρ = 780 мл × 1 гр/мл = 780 гр
2) Далее мы находим общую массу раствора:
m(общ. р-ра) = m(HOCH₂-CH(OH)-CH₂OH) + m(H₂O) = 24 гр + 780 гр = 804 гр
3) Далее мы находим массовую долю данного вещества в растворе по такой формуле:
ω(р-р в-ва) = m(вещества)/m(общ. р-ра) × 100%
m(вещества) = m(HOCH₂-CH(OH)-CH₂OH) = 24 гр
ω(р-р в-ва) = 24 гр/804 гр × 100% ≈ 0,03 × 100% ≈ 3%
ответ: ω(р-р в-ва) = 3%

2 водорода, 1 сера и 4 кислорода - всего 7 (ответ В)
2) Ломоносов (В)
3) фтор
e=p=9
n = 19 - 9 = 10 (ответ Г)
4) ковалентная связь это связь между неметаллами(полярная) и связь между одинаковыми атомами(неполярная)
такое только в ряде В вижу
5) W = m(в-ва)/m(р-ра) = 20/(180+20)=20/200=0.1 = 10% ответ Б
6) ответ Б, соединения, не ОВР
7) точно помню медь (Б), она стоит правей водорода, поэтому реакция с разб. кислотой не пойдет
8) конечно же, хлорид серебра (Г), это осадок и поэтому диссоциации практически не будет
9) вроде как Б (там у тебя две В, там где в ряде калий есть)
10) все вижу, кроме кислот (А)
11) там где ты видишь просто элемент,например сера или натрий напиши простое вещество
ОКСИД магния, сера, ОКСИД фосфора 5, серная КИСЛОТА, ГИДРОКСИД железа 3, натрий, ну напиши едкий калий (ГИДРОКСИД), фтороводородная КИСЛОТА, нитрат бария (СОЛЬ)
12)
Сера- электронная формула 1S2 2S2 2P6 3s2 3p4
Углерод - электронная формула 1s2 2s2 2p2
H2SO4, CO2
13)
1) Fe + Cl2 = FeCl2
2) FeCl2 + 2NaOH = 2NaCl + Fe(OH)2
3) Fe(OH)2 = FeO + H2O
4) FeO + H2 = Fe + H2O
14)
H2SO4 + 2NaOH = Na2SO4 + 2Н2О
n(H2SO4) = 24,5/98 = 0,25 моль
n(NaOH) = 2n(H2SO4) т.к. на 1 моль кислоты требуется 2 моля гидроксида = 0.5 моль
m(NaOH) = 0,5 * 40 = 20 г