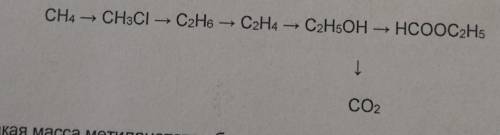
Водород - элемент с порядковым номером 1, его относительная атомная масса равна 1,008. Электронная формула атома водорода: 1s1.
Водород занимает двойственное положение в периодической системе элементов, его принято размещать и в I, и в VII группах (в галвных подруппах). Это обусловлено тем, что он имеет черты сходства и со щелочными металлами, и с галогенами. Как и атомы щелочных металлов, атом водорода может отдавать 1 электрон(окисляться) и превращаться в положительно заряженный электрон Н+. С другой стороны, как и атомы галогенов, атом водорода может присоединять 1 электрон (восстанавливаться) и превращаться в отрицательно заряженный гидрид-ион Н-.
Электроотрицательность водорода 2,1, что является промежуточной величиной ЭО типичных металлов и типичных неметаллов.
В своих соединениях водород обычно имеет степень окисления +1, реже -1.
тебе вот и ответ
1) CH4 + Cl2 =(уф.)=> CH3Cl + HCl
2) 2CH3Cl + 2Na =(t)=> 2NaCl + CH3-CH3
3) CH3-CH3 =(Ni, t)=> CH2=CH2 + H2
4) CH2=CH2 + H2O =(H3PO4, t)=> CH3-CH2OH
5) C2H5OH + 3O2 = 2CO2 + 3H2O
6) СH3CH2OH + HCOOH = HCOOC2H5 + H2O
Объяснение: