Типы реакций(превращение реагирующих частиц): соединения, разложения, замещения, обмена.
Реакция соединения. Реакция соединения - реакция, в результате которой из двух или нескольких менее простых веществ образуется одно более сложное вещество.(молекулы/атомы соединяются в одну молекулу)
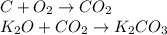
Реакция разложения. Реакция разложения - реакция, обратная реакции соединения. Полное определение: реакция, в результате которой из одного более сложного вещества получаются два или несколько менее простых веществ.(расщепление молекулы на атомы/молекулы)
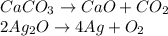
Реакция замещения. Реакция замещения - реакция, в результате которой атомы одного вещества замещают атомы другого вещества.(обмен атомами. не путать с реакцией обмена. в реакции обмена оба вещества сложные, а в замещения одно сложное, другое простое)
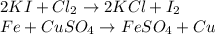
Реакция обмена. Реакция обмена - реакция, в результате которой вещества обмениваются своими составными частями(различие от реакции замещения сказано выше)
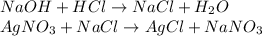
Например, анализ показал, что вещество является углеводородом CxHy, в котором массовые доли углерода и водорода соответственно равны 0,8 и 0,2 (80% и 20%). Чтобы определить соотношение атомов элементов, достаточно определить их количества вещества (число молей):
Целые числа (1 и 3) получены делением числа 0,2 на число 0,0666. Число 0,0666 примем за 1. Число 0,2 в 3 раза больше, чем число 0,0666. Таким образом, CH3 является простейшей формулой данного вещества.
Соотношению атомов C и H, равному 1 : 3, соответствует бесчисленное количество формул: C2H6, C3H9, C4H12 и т.д., но из этого ряда только одна формула является молекулярной для данного вещества, т.е. отражающей истинное количество атомов в его молекуле. Чтобы вычислить молекулярную формулу, кроме количественного состава вещества, необходимо знать его молекулярную массу. Для определения этой величины часто используется значение относительной плотности газа D.
Так, для вышеприведенного случая DH2 = 15.
Тогда M(CxHy) = 15 M(H2) = 15•2 г/моль = 30 г/моль.
Поскольку M(CH3) = 15, то для соответствия с истинной молекулярной массой необходимо удвоить индексы в формуле. Следовательно, молекулярная формула вещества: C2H6.
Определение формулы вещества зависит от точности математических вычислений. При нахождении значения ν элемента следует учитывать хотя бы два знака после запятой и аккуратно производить округление чисел. Например, 0,8878 ≈ 0,89 но не 1.
Соотношение атомов в молекуле не всегда определяется простым делением полученных чисел на меньшее число. Рассмотрим этот случай на следующем примере.
Задача 1. Установите формулу вещества, которое состоит из углерода (ω=25%) и алюминия (ω=75%).
Разделим 2,08 на 2. Полученное число 1,04 не укладывается целое число раз в числе 2,78 (2,78 : 1,04 = 2,67 : 1). Теперь разделим 2,08 на 3. При этом получается число 0,69, которое укладывается ровно 4 раза в числе 2,78 и 3 раза в числе 2,08. Следовательно, индексы x и y в формуле вещества AlxCy равны 4 и 3, соответственно.
ответ: Al4C3 (карбид алюминия).
Более сложным вариантом задач на вывод формул соединений является случай, когда состав вещества задается через продукты сгорания этих соединений.
Задача 2. При сжигании углеводорода массой 8,316 г образовалось 26,4 г CO2. Плотность вещества при нормальных условиях равна 1,875 г/мл. Найдите его молекулярную формулу.