Дано:
а)m(P2O5)=71г
б)m(CO2)=4.4 г
в)m(MgO)=4г
г) m(NO)=4.5 г
------------------------------
m(O2)=?(г)
Решение:
а) 4P+ 5O2= 2P2O5
n(P2O5)=m/Mr=71г/142г/моль=0.5 моль
n(O2)=5/2n(P2O5)=1.25 моль
m(O2)=n x Mr=1.25моль х 32г/моль=40г
б) С + O2 = CO2
n(CO2)=m/Mr=4.4г/44г/моль=0.1 моль
n(O2)=n(CO2)=0.1 моль
m(O2)=n x Mr= 0.1 моль х 32г/моль=3.2г
в) 2Mg+O2=2MgO
n(MgO)=m/Mr=4г/40г/моль=0.1 моль
n(O2)=0.5n(MgO)=0.05 моль
m(O2)=n x Mr=0.05 моль х 32 г/моль=1.6 г
г) N2 + O2 = 2NO
n(NO)=m/Mr=4.5 г/30г/моль=0.15 моль
n(O2)=0.5 n(NO)=0.075моль
m(O2)=n x Mr=0.075моль х 32г/моль=2.4 г
ответ: а) 40 г б)3.2г в)1.6 г г)2.4 г
Если нажми кнопку
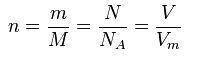
Все соли образованы кислотой и основанием.
1) Если кислота и основание сильное, то соль гидролизу не подвергается, среда раствора этой соли - нейтральная, pH = 7.
Например: NaCl образован сильной кислотой HCl и сильным основанием NaOH. Значит он не подвергается гидролизу, среда нейтральная, pH = 7.
2) Если кислота слабая, а основание сильное, то соль подвергается гидролизу по аниону, среда раствора этой соли - щелочная, рН > 7.
Например: Na2CO3 образован слабой кислотой H2CO3 и сильным основанием NaOH. Значит соль подвергается гидролизу по аниону, среда щелочная, рН > 7:
Na2CO3 + 2H2O = H2CO3 + 2NaOH
CO3(2-) + 2H2O = H2CO3 + 2OH(-)
3) Если кислота сильная, а основание слабое, то соль подвергается гидролизу по катиону, среда раствора этой соли - кислая, рН < 7.
Например: FeCl3 образован сильной кислотой HCl и слабым основанием Fe(OH)3. Значит соль подвергается гидролизу по катиону, среда кислотная, рН < 7:
FeCl3 + 3H2O = Fe(OH)3 + 3HCl
Fe(3+) + 3H2O = Fe(OH)3 + 3H(+)
4) Если и кислота, и основание слабые, то соль подвергается гидролизу и по катиону, и по аниону. Среда раствора такой соли зависит от соотношения сил кислоты и основания (если кислота сильнее основания, то среда - слабокислая; если основание сильнее, то среда слабощелочная).
Например: CH3COONH4 образован слабой кислотой CH3COOH и слабым основанием NH4OH. Значит соль подвергается гидролизу и по катиону, и по аниону:
CH3COONH4 + H2O = CH3COOH + NH4OH
CH3COO(-) + NH4(+) + H2O = CH3COOH + NH4OH
Если и кислота, и основание - очень слабые электролиты, то часто такие соли полностью гидролизуются в воде.
Например: Al2S3 образован очень слабой кислотой H2S и очень слабым основанием Al(OH)3. Соль полностью гидролизуется:
Al2S3 + 6H2O = 2Al(OH)3 + 3H2S
(Ионное уравнение совпадает с молекулярным)
Можно обратить внимание на то, что гидролиз по сути является обратной реакцией по отношению к реакции нейтрализации.
Если слабые кислота или основание диссоциируют ступенчато, то гидролиз протекает ступенчато. Например:
Гидролиз Na2CO3:
1-ая ступень: Na2CO3 + H2O = NaHCO3 + NaOH
CO3(2-) + H2O = HCO3(-) + OH(-)
2-ая ступень: NaHCO3 + H2O = H2CO3 + NaOH
HCO3(-) + H2O = H2CO3 + OH(-)
Гидролиз FeCl3:
1-ая ступень: FeCl3 + H2O = FeOHCl2 + HCl
Fe(3+) + H2O = FeOH(2+) + H(+)
2-ая ступень: FeOHCl2 + H2O = Fe(OH)2Cl + HCl
FeOH(2+) + H2O = Fe(OH)2(+) + H(+)
3-ья ступень: Fe(OH)2Cl + H2O = Fe(OH)3 + HCl
Fe(OH)2(+) + H2O = Fe(OH)3 + H(+)
Гидролиз преимущественно протекает по 1-ой ступени и редко протекает до конца.
Следует обратить внимание еще на один факт. Гидролиз - обратимая реакция.