1. Найдем через плотность относительную молекулярную формулу вещества:
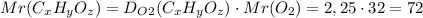
2. Теперь,вспомнив формулу по вычислению массовой доли элемента в веществе и выведя из нее n - количество атомов элемента,найдем количество атомов каждого:
а) n(C)=Mr(C_xH_yO_z)*w(C)/Ar(C)*100%=72*66,67/12*100=4
б) n(H)=Mr(C_xH_yO_z)*w(H)/Ar(H)*100%=72*11,11/1*100=8
в) n(O)=Mr(C_xH_yO_z)*w(O)/Ar(O)*100%=72*22,22/16*100=1
Выходит простейшая формула: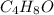
Если подставлять в общие формулы кислородсодержащих соединений,то получим: -это бутаналь
-это бутаналь
№1.CaCO3 + HCL → CaCL2 + CO2↑ + H2O (ур+ пол.ион.)
При пропускании газа через известковую воду происходит две последовательные реакции:
А) образование белого осадка:
CO2 + Ca(OH)2→ CaCO3↓ + H2O (полн.ион.ур)
Б) растворение осадка:
CaCO3 + CO2 + H2O → Ca(HCO3)2 ( полн.ион.ур)
№2. Пропускаем углекислый газ через дистиллированную воду и добавляем раствор лакмуса.
Лакмус краснеет, так как образуется слабая кислота:
CO2 + H2O ↔ H2CO3
№3. Пропускаем CO2 через раствор NaOH с ф/ф.
Малиновый раствор обесцветился, произошла реакция нейтрализации:
NaOH + CO2 → Na2CO3 + H2O (ур.+ полн.ион.ур)
Na2CO3 + CO2 + H2O → NaHCO3(ур + полн.ион.ур)
K2CO3 + HCL →KCL + CO2↑ + H2O ( ур + полн.и сокр.ион.ур)
Na2SiO3 + HCL → NaCL + H2SiO3↓ ( ур + полн.и сокр.ион.ур)
Na2SO4 + BaCL2 → BaSO4↓ + NaCL ( ур + полн.и сокр.ион.ур)
ZnCL2 + AgNO3 → AgCL + Zn(NO3)2 ( ур + полн.и сокр.ион.ур)
Вывод: в ходе выполнения практической работы мы получили CO2↑ , рассмотрели его свойства и с характерных реакций распознали неизвестные вещества.
Hope everything will be understandable