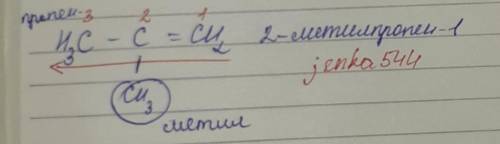Школьные Знания.com
Какой у тебя во классы Химия 32+16 б НУЖНА ХИМИЯ 50 баллов
1.Какая масса анилина может быть получена из 200 см3 бензола(р=0,88г/см3) если выход на стадии нитрования 80% а на стадии восстановления 70%
2.Какую массу анилина можно получить двухстадийным синтезом из бензола массой 23.4 г если выход на каждой стадии равен 80%
Отметить нарушение Chesyameleri 13.05.2018
ответы и объяснения
Alexei78
Alexei78Модератор-Стажер
дано
V(C6H6) = 200 cm3
p(C6H6) = 0.88 g/cm3
η(C6N5NO2) = 80%
η(C6H5NH2) = 70%
m(С6H5NH2)-?
m(C6H6) = p(C6H6)*V(C6H6) = 0.88 * 200 = 176 g
176 X
C6H6+HNO3-->C6N5NO2+H2O
78 123
M(C6H6) = 78 g/mol
M(C6H5NO2) = 123 g/mol
X = 176*123 / 78 = 277.54 g
Находим массу практическую с учетом выхода первой стадии
m(C6H5NO2) = 277.54 * 80% / 100% = 220 .032 g
220.032 X
C6H5NO2+3H2-->C6H5NH2+2H2O
123 93
M(C6H5NH2) = 93 g/mol
X = 220.032 * 93 / 123 = 166.58 g
Находим массу практическую с учетом выхода второй стадии
m(C6H5NH2) = 166.58 * 70% / 100% = 116.6 g
ответ 116.6 г
2)
дано
m(C6H6) = 23.4 g
η1(C6H5NO2) = 80%
η2(C6H5NH2) = 80%
m(C6H5NH2)-?
23.4 X
C6H6+HNO3-->C6N5NO2+H2O
78 123
M(C6H6) = 78 g/mol
M(C6H5NO2) = 123 g/mol
X = 23.4*123 / 78 = 36.9 g
Находим массу практическую с учетом выхода первой стадии
m(C6H5NO2) = 36.9 * 80% / 100% = 29.52 g
29.52 X
C6H5NO2+3H2-->C6H5NH2+2H2O
123 93
M(C6H5NH2) = 93 g/mol
X = 29.52 * 93 / 123 = 22.32 g
Находим массу практическую с учетом выхода второй стадии
m(C6H5NH2) = 22.32 * 80% / 100% = 17.856 g
ответ 17.856 г
Объяснение:
2-метилпропен-1
Объяснение:
1. Выделяют в формуле наиболее длинную связь,содержащую двойную связь. Нумерацию атомов начинают с того конца,к которому ближе двойная связь. В нашем случае,будем выбирать прямолинейно длинную связь,ведь кривлять её нет смысла. В основе у нас лежит пропен, из трёх атомов углерода. Нумеруем с правого конца и влево,потому что двойная связь там ближе.
2. В начале названия соединения указывают цифрой,при каком атоме углерода находится заместитель. У нас на втором атоме углерода идёт разветвление и радикал один называется метил. Так и пишем, 2-метилпропен.....
3. После названия длинной цепи обозначают положение двойной связи при том атоме углерода,от которого начинается двойная связь.
Получается у нас 2-метилпропен-1.
*Название радикалов и алкенов образуются от первых представителей -алканов. В случае с радикалами,суффикс ан заменяется на ил. Получается:метил,этил,пропил....и т.д . В случае с алкенами,суффикс ан заменяется на ен. Получается:пропен,пентен,гексен....и т.д.