1)Находим массу чистого вещества(без примесей)
500 000 г-100%
хг -30%
х=500 000 * 30%/100%= 150 000 г (это масса примесей)
m(чистого в-ва)=500 000 - 150 000= 350 000 г
2) Уравнение реакции:
350 000 г х л
CaCO3 + 2HCl> CaCl2 + CO2(стрелка вверх) +H2O
M=100г/моль Vm= 22,4л/моль
m=100 г V=22,4л
Пропорция: 350 000/100=x/22,4
=> x=350 000*22,4/100= 78 400 л
3)Рассчитаем кол-во вещества газа:
Формула: v=V/Vm
v(CO2)=78 400 л/22,4 л/моль= 3500 молей.
Овет:78 400 л; 3 500 молей.
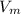 * n = 22,4 м³/кмоль * 3,5 кмоль = 78,4 м³
* n = 22,4 м³/кмоль * 3,5 кмоль = 78,4 м³
BaCO₃ + 2HCl = BaCl₂ + CO₂ + H₂O
197г. 208г. 22,4л. 18г.
197г.BaCO₃ - 22.4л.CO₂
112гBaCO₃ - Хл CO₂ Х= 112 х 22.4÷197=12.7 л.CO₂
197г.BaCO₃ - 18г.H₂O
112гBaCO₃ - Хг.H₂O Х= 112х18÷197=10.2г.H₂O
197г.BaCO₃ - 208г. BaCl₂
112гBaCO₃ - Хг. BaCl₂ Х= 112х208÷197=118.2гBaCl₂.
118.2г.÷197г.= 0,6 моль
1моль BaCO₃ - 6·10²³ молекул
0,6мольBaCO₃ - Х молекул Х= 0,6 х 6·10²³÷1 = 3,6·10²³ молекул BaCO₃