Для приготовления раствора методом навески сухого вещества,необходимо найти массу карбоната калия,которую необходимо растворить в Н2О. Соответственно массу нужно вычислить n экв К2CO3= Сэкв * V(Л) 100мл=0,1л n экв К2CO3= 0,1*0,1=0,01 моль-экв так как фактор эквивалентности карбоната калия равен 0,5,то n= 0,01/0,5= 0,02моль М (К2CO3)= 138г/моль m. (К2CO3)=n*M= 138* 0,02=2,76г Для приготовления 100 мл 0,1 Н раствора К2CO3 нужно взвесить 2,76г К2CO3 и растворить в 100мл дистиллированной воды.
Объяснение:
Объяснение:
Окислитель и восстановитель определяются в реакции, а не в чистом веществе.
Возьмем на пример реакцию разложения твоего вещества CrO3.
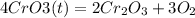
Теперь надо расставить степени окисления каждого элемента:
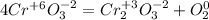
Теперь мы можем видеть как изменились степени окисления.
Если элемент принимает электроны то он окислитель, а процесс восстановления. Степень окисления уменьшается.
Если элемент отдает электроны то восстановитель, а процесс окисления. Степень окисления увеличивается.
Теперь рассмотрим как поменялись степени окисления:
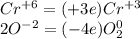
Как можем видеть 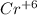 окислитель, а
окислитель, а 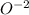 восстановитель
восстановитель
3LiNO3 + Na3PO4 = Li3PO4 + 3NaNO3
3Li(+) + 3NO3(-) + 3Na(+) + PO4(-3) = Li3PO4 + 3Na(+) + 3NO3(-)
3Li(+) + PO4(-3) = Li3PO4