ответ: 28,7 г
Объяснение:
2AgNO3 + MgCl2 = 2AgCl↓ + Mg(NO3)2
m(AgNO3) = 34г
M(AgNO3) = 170 г/моль
M(AgCl) = 143,5 г/моль (хлор всегда берём как 35,5)
m(MgCl2) = 19г
M(MgCl2) = 95 г/моль
n(AgNO3) = m/M = 0,2 моль
n(MgCl2) = m/M = 0,2 моль
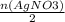 = 0,1 <
= 0,1 < 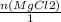 = 0,2
= 0,2
значит, n(AgCl) = n(AgNO3) = 0,2 моль
m(AgCl) = n*M = 0,2 * 143,5 = 28,7г
Если даны массы нескольких исходных веществ, то расчет по уравнению реакции проводят по тому из веществ, которое находится в недостатке, т.е. первым заканчивается в реакции.
Для того, чтобы узнать, какое из веществ находится в недостатке, сравнивают их относительные количества, т.е. количества, деленные на соответствующие коэффициенты в уравнении реакции.
В.Хлорид Калия
3)Утверждение,характерное для истинных растворов
В.МЕжду частицами дисперсионной среды и дисперсной фазы не существует поверхности раздела
5)Вещества, не образующие при взаимодействии коллоидный раствор:
А.Оксид кремния (4) и гидроксид калия(плавление)
7)Система, не обрзующая коллоиды
Г.Газ-Газ
10)Объем газа (н.у) образующегося при взаимодействии 0.02 моль натрия с водой, равен
Г.224мл