х г 4 г
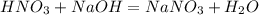
63 г 40 г
1. Сначала найдем чистую массу кислоты которая ушла на нейтрализацию 4 г гидроксида:
для полного взаимодействия 63 г кислоты необходимо 40 г гидроксида, а
для -- // -- х г____________________4 г, откуда
х=63*4/40=6,3 г
2. Теперь эту массу отнесем к массе всего раствора,которая дается по условиям задачи и равна 200 г(поэтому в дано запиши правильно:m(раствора)=200 г):
w(HNO3)=m(HNO3)/m(раствора)=6,3/200=0,03 или 3%
4 моль Х г
2HgO = 2Hg + O2
n = 2 моль n = 1 моль
Mr = 32 г/моль
m = 32 г
4 моль HgO - Х г О2
2 моль HgO - 32 г О2
m(O2) = 4 * 32 / 2 = 64 г