При окислении увеличивается, при восстановлении уменьшается.
Сa+O2=2CaO.
Ca(0)-2e=Ca(2+) окисление
O2(0)+4e=2O(2-) восстановление.
0 / 0
Степень окисления может повышаться и понижаться в зависимости от процесса протекания реакции.
Если элемент окисляется - то степень будет повышаться.
Если элемент востанавливается, то степень будет понижаться
окисление элемент окислитель забирает электроны и присоединяет их к себе. окислитель имеет знак -, восстановитель- элемент отдающий элетроны, знак + например NaCl- натрий имеет знак + т. к. металл и является восстановителем, хлор имеет -, т. к окислитель
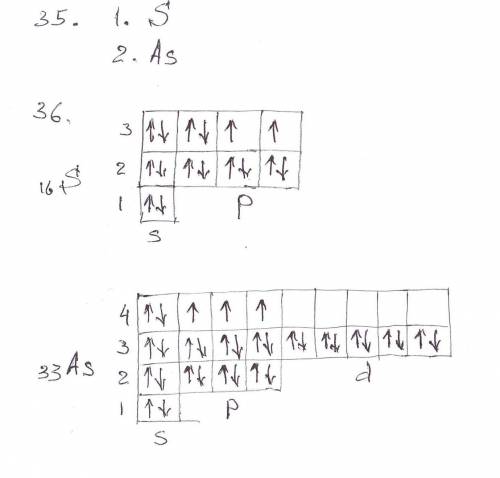
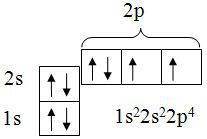
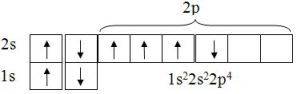
36. Дописать название подуровня и его номер. Записать химический знак элемента и перед ним поставить его порядковый номер. (См. в файл)
37. Номеру данного периода.
38. Номеру группы.
39. Количеством валентных электронов, т.е. электронов на внешнем слое.
40. Изменением строения их электронных оболочек. В каждом периоде происходит заполнение электронами внешнего энергетического уровня до восьми. Следовательно, электронные конфигурации наружных энергетических уровней периодически повторяются.
41. s-элементы - это элементы главной подгруппы I и II групп. По факту это элементы у которых заполняется s-уровень. В каждом периоде по 2 s-элемента.
42. р-элементы - это элементы III-VIII групп, главных подгрупп. Это элементы у которых заполняется р-уровень. Всего 6 р-элементов в каждом периоде (кроме первого, их там нет; и седьмого - хотя там тоже их 6 штук).
43. d-элементы - это элементы I-VIII групп, побочных подгрупп. Это элементы у которых заполняется d-уровень. В каждом большом периоде по 10 d-элементов.
Объяснение: