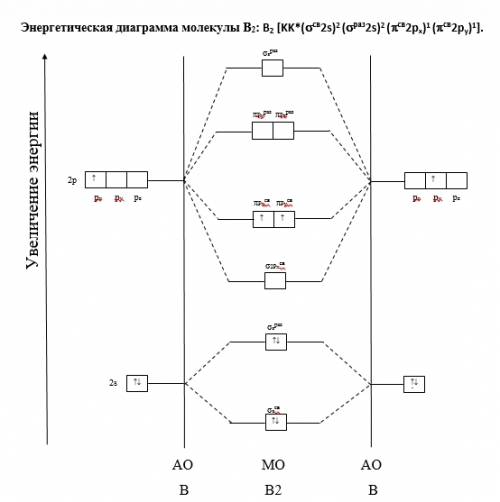
Дано:
а)m(P2O5)=71г
б)m(CO2)=4.4 г
в)m(MgO)=4г
г) m(NO)=4.5 г
------------------------------
m(O2)=?(г)
Решение:
а) 4P+ 5O2= 2P2O5
n(P2O5)=m/Mr=71г/142г/моль=0.5 моль
n(O2)=5/2n(P2O5)=1.25 моль
m(O2)=n x Mr=1.25моль х 32г/моль=40г
б) С + O2 = CO2
n(CO2)=m/Mr=4.4г/44г/моль=0.1 моль
n(O2)=n(CO2)=0.1 моль
m(O2)=n x Mr= 0.1 моль х 32г/моль=3.2г
в) 2Mg+O2=2MgO
n(MgO)=m/Mr=4г/40г/моль=0.1 моль
n(O2)=0.5n(MgO)=0.05 моль
m(O2)=n x Mr=0.05 моль х 32 г/моль=1.6 г
г) N2 + O2 = 2NO
n(NO)=m/Mr=4.5 г/30г/моль=0.15 моль
n(O2)=0.5 n(NO)=0.075моль
m(O2)=n x Mr=0.075моль х 32г/моль=2.4 г
ответ: а) 40 г б)3.2г в)1.6 г г)2.4 г
Если нажми кнопку
Если даны р-ры веществ,то в р-ре (NH4)2SO4 среда кислотная,в р-ре NaCl среда нейтральная.
Это можно опрелелить с индикатора.И так,предварительно мы распознали. Дальше необходимо все-таки провести качественные р-ции:
на анионы:1)SO4(2-) +Ba(2+)=BaSO4-осадок белый кристаллический
2)Cl(-) +Ag(+)=AgCl-осадок белый творожистый
на катионы:1)NH4(+) +OH(-)=NH3+H2O-газ с резким запахом.
Если соли твердые,то при нагревании ( NH4)2SO4=2NH3+SO3+H2O(резкий запах аммиака)
NaCl окрашивает пламя спиртовки в желтый цвет(Na(+) окрашивают).