98,4 г х л
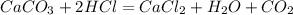
100 г 22,4 л
1.Сначала найдем чистую массу карбоната кальция в мраморе,зная,что в последнем содержится 18% примесей:
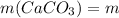 (мрамора)
(мрамора)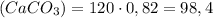 г
г
2. Теперь,подставив эту массу в уравнение реакции,определим объем углекислого газа:
При взаимодействии 100 г карбоната выделяется 22,4 л углекислого газа, а
при -- // -- 98,4 г___________________х л, откуда
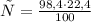 =22,04 л
=22,04 л
2. HOCl + H2O2 = HCl + O2 + H2O
Объяснение:
Все реакции окислительно-восстановительные, значит должен быть элемент который обязательно понизит степень окисление(как в этом примере Cl(+1) -> Cl(-1)), и который повысит(2O(-1) -> O2(0)).
Надо примерно понять, что может получиться в продуктах, и что нужно добавить в реагенты(иногда воду)
Также не стоит забывать свойства KMnO4 и K2Cr2O7. Т.к. надо знать что будет образовываться в продуктах, используя эти окислители.
Cr - во всех средах будет понижать с.о. до +3
Mn - в кислой до +2, в нейтральной до +4, в щелочной до +6
->H2NCH(CH3)CONHCH(CH2SH)COOH+H2O