16.9%
Объяснение:
Пишем первую реакцию
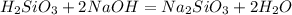
Считаем массу гидроксида натрия
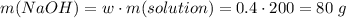
Считаем количество вещества кремниевой кислоты
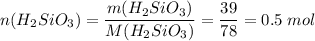
Для реакции нужно вдвое больше гидроксида натрия, т.е. 1 моль или 40 г, а есть 80 г, поэтому расчеты ведем по кремниевой кислоте
Силиката натрия образуется столько же, сколько и было кремниевой кислоты, т.е. 0.5 моль
Пишем вторую реакцию
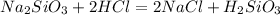
Для полного взаимодействия с 0.5 моль силиката натрия нужно 1 моль кислоты, т.е. 36.5 г. Считаем сколько есть
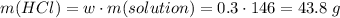
Видим, что соляной кислоты в избытке, поэтому расчеты ведем по силикату натрию
Во время реакции образуется 1 моль хлорида натрия, т.е. 58.5 г и 0.5 моль кремниевой кислоты, т.е. 39 г, которая выпадает в осадок и в массе раствора не считается
Считаем всю массу раствора
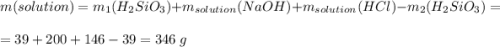
Считаем массовую долю хлорида натрия

1. Б) 90
2.А) 2
3. Б) NO, H2S, PH3, Cl2O7
4. Б) азота
5. Б) 66 г
6. А) 11,2 л
7. ТУТ ДОЛЖНО БЫТЬ 1 МОЛЬ
8. Б) 0,3 моль
9. А) CrO3
10.Б) HNO3, Na2CO3, P2O5
11.Б) F2O7, CO, P2O5 (только тут СО -он несолеобразующий оксид. Но другие варианты не подходят)
12.
Сa(OH)2 + 2HNO3 = Ca(NO3)2 + 2H2O
А) 4
13.Б) алюминий
14.Г) замещения
15.А) водородом и кислородом
Часть 2
16. Решите цепочку превращений Na – NaOH – Na2SO4
2Na+2H2O=2NaOH+H2
2NaOH+H2SO4=Na2SO4+2H2O
17.Сколько соли и воды нужно взять для приготовления 10 гр 10% раствора соли?
m(соли)=10г*10%/100%=1 г соли
m(H2O)=10г-2г=9г воды
18. Запишите уравнение реакции взаимодействия сульфата железа (III) и гидроксида калия.
Fe2(SO4)3+6KOH=2Fe(OH)3+3K2SO4