Увеличение давления в системе в 2 раза равносильно уменьшению объема системы в 2 раза. При этом концентрации реагирующих веществ возрастут в 2 раза. Согласно закону действия масс, начальная скорость реакции равна vн=k·[N2]·[H2]3. После увеличения давления в 2 раза концентрации азота и водорода увеличатся в 2 раза, и скорость реакции станет равна vк=k·2[N2]·23[H2]3=k·32[N2]·[H2]3. Отношение vк./vн показывает, как изменится скорость реакции после изменения давления. Следовательно, vк/vн=k·32[N2]·[H2]3/(k·[N2]·[H2]3)=32.
ответ: скорость реакции увеличится в 32 раза.
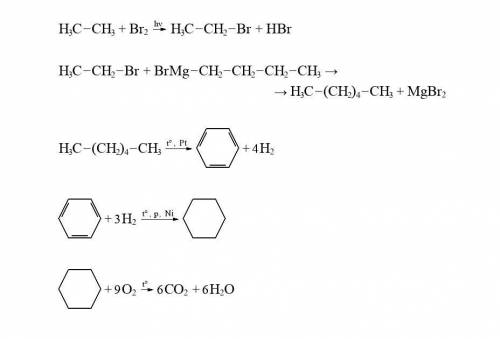
1) Этан (алкан) реагирует с бромом при УФ, получается бромэтан и бромоводород
Галогенирование заместительное
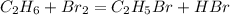
2) Бромэтан взаимодействует с бутилмагнийбромидом получается гексан и бромид магния
Синтез Гриньяра
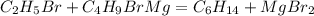
3) Гексан при температуре и катализаторе разлагается на бензол (арен) и водород
Дегидроциклизация
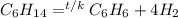
4) Бензол взаимодействует с водородом при высоком давлении, температуре и катализаторе, получается циклогексан (циклоалкан)
Гидрирование аренов
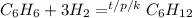
5) Циклогексан горит в кислороде, получается вода и углекислый газ
Горение
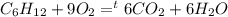
n(Al)=10.95/27=0.4моль
n(HCl)=109.5*0.1=10.95/36.5=0.3
0.4/2=0.2
0.3/6=0.05
алюминий дан в избытке,расчет ведем по HCl
m(AlCl3)=0.05*2*133.5=13.25г
V(H2)=0.05*3*22.4=3.36л
m(непрореагирующего Аl)=0.05*2*27=7.3г
m(H2O)=109.5*0.9=98.55г
ответ: m(AlCl3)=13.25. V(H2)3.36. m(Al)7.3. m(H2O)98.55