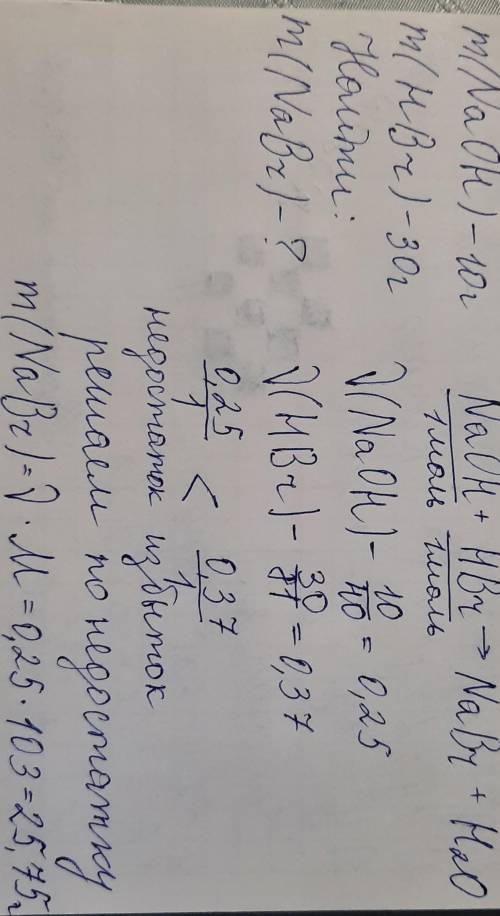ответ: 3,2 мл; 2 л О2
Дано:
V(H2)=4 л
V(O2) = 4 л
V(H2O)-?
V(г.)-?
Объяснение:
M(H2O) = 18 г/моль
2Н2 + О2 = 2Н2О
Из УХР V(H2):V(O2) = 2:1, исходя из условия задачи V(H2):V(O2) = 2:2, кислород взят в избытке, 4 л водорода вступят в реакцию с 2 л кислорода, 2 л кислорода выделится после реакции.
n(H2) = 4 л/22,4 л/моль = 0,1786 моль, из УХР видно, что n(H2O) = n(H2)
n(H2O) = 0,1786 моль
m(H2O) = n*M = 0,1786 моль*18 г/моль = 3,2 г
ρ(Н2О) = 1 г/мл
V(H2O) = m(H2O)/ρ(Н2О) = 3,2 г/1 г/мл = 3,2 мл
ответ: 3,2 мл; 2 л О2
ответ: 25,75 г
Дано:
m(NaOH) = 10 г
m(HBr) = 30 г
m(NaBr)-?
Объяснение:
M(NaOH) = 40 г/моль
M(HBr) = 81 г/моль
M(NaBr) = 103 г/моль
n=m/M
n(NaOH) = 10 г/40 г/моль = 0,25 моль
n(HBr) = 30 г/81 г/моль = 0,37 моль
Составляем УХР:
NaOH + HBr = NaBr + H2O
Из УХР следует, что n(NaOH):n(HBr) = 1:1, исходя из расчетов по условию задачи n(NaOH):n(HBr) = 0,25:0,37 = 1:1,48, следовательно, бромоводородная к-та взята в избытке, расчеты ведем по гидроксиду натрия: из УХР видно, что n(NaBr) = n(NaOH); n(NaBr)=0,25 моль
Находим массу соли - бромида натрия:
m(NaBr) = n(NaBr)*M(NaBr) = 0,25 моль*103 г/моль = 25,75 г
ответ: 25,75 г