Начнем - с.
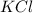 - соль сильного основания - KOH, и сильной кислоты - HCl - гидролизу не подвергается.
- соль сильного основания - KOH, и сильной кислоты - HCl - гидролизу не подвергается.
 - соль сильного основания - KOH, и слабой кислоты -
- соль сильного основания - KOH, и слабой кислоты - 
Гидролиз пойдет по аниону - 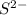
1 - ступень:
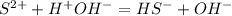 Гидроксид - аноины говорят нам о том, что среда - щелочная - лакмус синий
Гидроксид - аноины говорят нам о том, что среда - щелочная - лакмус синий
Молекулярный Вид: 
2 - ступень:
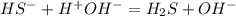 - снова щелочная среда, лакмус - синий
- снова щелочная среда, лакмус - синий
Молекулярный вид: 
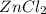 - соль слабого основания -
- соль слабого основания - 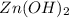 , сильной кислоты - HCl
, сильной кислоты - HCl
гидролиз пойдет по катиону - 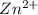
1 - ступень:
 <- катионы водорода говорят нам о том, что среда раствора кислая, лакмус - красный.
<- катионы водорода говорят нам о том, что среда раствора кислая, лакмус - красный.
МВ: 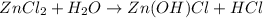
2 - ступень:
 <- снова катиончики водорода говорят нам о том, что среда кислая, а лакмус краснеет.
<- снова катиончики водорода говорят нам о том, что среда кислая, а лакмус краснеет.
МВ: 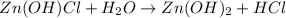
 - соль слабого основания, сильной кислоты - гидолизируется по катиону:
- соль слабого основания, сильной кислоты - гидолизируется по катиону:
1 - ступень:
 <- катионы водорода, говорят нам о том, что среда кислая, лакмус - красный.
<- катионы водорода, говорят нам о том, что среда кислая, лакмус - красный.
МВ: 
2 - ступень:
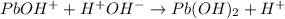 <- среда кислая, лакмус - красный
<- среда кислая, лакмус - красный
МВ: 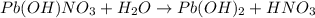
 - соль сильного основания, слабой кислоты, гидролиз по аниону.
- соль сильного основания, слабой кислоты, гидролиз по аниону.
1 - ступень:
 среда щелочная, лакмус синий
среда щелочная, лакмус синий
МВ: 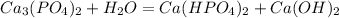
2 - ступень:
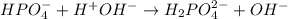
МВ: 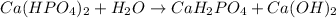
3 - ступень:

МВ: 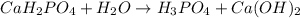 среда щелочная, лакмус синий
среда щелочная, лакмус синий
 - соль сильного основания, слабой кислоты - гидролиз по аниону.
- соль сильного основания, слабой кислоты - гидролиз по аниону.
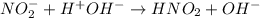 <- гидроксид - анионы угазывают на щелочной характер среды, лакмус синеет.
<- гидроксид - анионы угазывают на щелочной характер среды, лакмус синеет.
МВ: 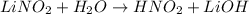
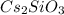 - соль сильного основания, слабой кислоты, гидролиз по аниону:
- соль сильного основания, слабой кислоты, гидролиз по аниону:
1 - ступень:
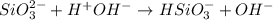 <- снова среда щелочная, лакмус синий
<- снова среда щелочная, лакмус синий
МВ: 
2 ступень:
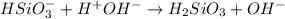
МВ: 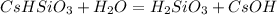
 - соль сильной кислоты, слабого основания, гидролиз по катиону:
- соль сильной кислоты, слабого основания, гидролиз по катиону:
1 - ступень:
 среда кислая, лакмус красный
среда кислая, лакмус красный
МВ: 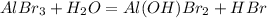
2 - ступень:
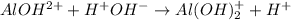
МВ: 
3 - ступень

МВ: 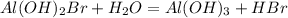
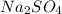 - соль сильного основания, сильной кислоты - гидролизу не подвергается, среда - нейтральная, лакмус - фиолетовый
- соль сильного основания, сильной кислоты - гидролизу не подвергается, среда - нейтральная, лакмус - фиолетовый
Объяснение:
2KClO3 ---> 2KCl + 3O2 (1)
4KClO3 ---> KCl + 3KClO4 (2)
Общее количество разложившегося хлората калия (бертолетовой соли) равно 14,7:123 = 0,12 моль. Пусть по уравнению (1) разложилось х моль хлората калия. Тогда по уравнению (2) разложилось (0,12 - х) моль, и количество выделившегося водорода равно 3х/2 = 1,5*х моль.
Хлорид-ионов образовалось х моль (по уравнению 1) и (0,12 - х)/4 = 0,03 - 0,25*х моль (по уравнению 2) , а перхлорат-ионов по уравнению (2) получилось 3*(0,12 - х)/4 = 0,75*(0,12 - х) = 0,09 - 0,75*х моль. По условию их количества одинаковы, тогда:
0,09 - 0,75*х = х + 0,03 - 0,25*х, откуда х = 0,04 моль.
Объём выделившегося кислорода при н.у. составит 1,5*0,04*22,4 = 1344 мл.
Условия: t до 100C
2)
A) 5HCOOH + 2KMnO4 + 3H2SO4=> K2SO4 + 2MnSO4 + 5CO2↑ + 8H2O
Б) Са(OH)2 + 2CO2 = Ca(HCO3)2
Условия - при комнатной температуре
3)
CH₃-(CH₂)₇-CH=CH-(CH₂)₇-COOH + Br₂ =>
=> CH₃-(CH₂)₇-CHBr-CHBr-(CH₂)₇-COOH
бромная вода обесцвечивается за счет того, что в углеродной цепи олеиновой кислоты имеется двойная связь, бром вступает в реакцию, образуя 9,10-дибромстеариновую кислоту.