Привет! Сейчас решим
1. Сера в природе встречается в самородном виде, а также входит в состав сульфидов и сульфатов. Например, цинковая обманка – ZnS, FeS2 – пирит, Cu2S – медный колчедан.
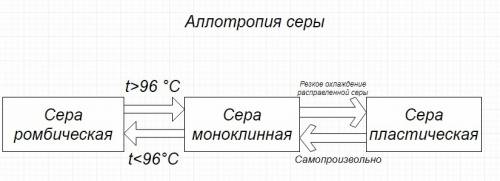
2. Существует несколько аллотропных модификаций серы. Ромбическая представляется собой желтый порошок с tпл = 113 – наиболее устойчивая форма серы. При 96 градусах ромбическая сера превращается в моноклинную. Она уже представляет собой темно-желтые иглы. Если их расплавить и резко охладить, получим серу пластическую – коричневую резиноподобную массу. Она неустойчива и постепенно превратится в ромбическую серу, когда полностью остынет.
3. Сера более электроотрицательный элемент, по сравнению с металлами, поэтому она отнимать электроны у последних, приобретая отрицательную степень окисления. А вот галогены и кислород более электроотрицательны, чем сера. Поэтому, они уже у серы отнимают электроны, и возникает положительная степень окисления.
4. Составим уравнение химической реакции. S + O2 = SO2
Как видно из уравнения, для сжигания 1 моль серы требуется 1 моль кислорода. n(S) = 4:32 = 0,125 моль. n(O2) = 0,125 моль. V(O2) = 22,4*0,125 = 2,8 литра. V(возд) = 2,8:0,2 = 14 литров
5. Поскольку серы увеличивает свою степень окисления от -2 (H2S) до +6 (SO3), окислительные свойства растут, а восстановительные – снижаются. Наиболее сильный окислитель – SO3, восстановитель – H2S.
6. S + O2 = SO2 + 332,8 кДж. Из уравнения реакции видно, что при окислении 1 моль серы выделяется 332,8 кДж тепла. n(S) = 1:32 = 0,03125 моль. Q = 0,03125*332,8 = 10,4 кДж
7. Краткая схема представлена во вложении
Готово!
2( в третьому ступені)= 2*2*2=8
Відповідь: в 8 раз
4. V-C/t
C=C1- C2= 0.068-0.064=0.004
V=0.004/5=0.0008 моль/хв
5. 0,2 x
H2SO4+K2CO3=K2SO4+CO2+H2O
1 1
m(K2CO3)=m(rasvora)*w=110*0,25=27,5 gramm
n(K2CO3)=m/M=27,5/138=0,2 moll
n(CO2)=x=0,2*1/1=0,8 moll
V(CO2)=Vm*n=22,4*0,2=4,48 dm3
Відповідь: 4,48 dm3.