Відповідь:Дано:
m[(NH₄)₂SO₄] =33г.
Vm= 22,4л./моль
NH₃
V(NH₃)-?
1. Определим молярную массу амонiй сульфату:
M[(NH₄)₂SO₄]=(14+1x4) + 32+16x4=114г./моль
2. Определим количество вещества n амонiй сульфату в его массе 33г.
n[(NH₄)₂SO₄] =m[(NH₄)₂SO₄] ÷M[(NH₄)₂SO₄]= 33г.÷114г./моль=0, 29моль
3. Запишем уравнение реакции взаимодействия амонiаку с сульфатною кислотою: 2NH₃ + H₂SO₄ = (NH₄)₂SO₄
4. Анализируем уравнение реакции: по уравнению реакции образовалось 1моль амонiй сульфату из 2моль амонiаку, значит если образовалось 0,29моль амонiй сульфату, то в реакцию должно вступить в два раза больше моль амонiаку.
n(NH₃)=0.29мольх2=0,58моль
5. Определим объем амонiаку количеством вещества 0,58моль:
V(NH₃) =n(NH₃)xVm=0,58мольх 22,4л./моль=12,99л.
6. ответ: для получения 33г. амонiй сульфату потребуется 12,99л. амонiаку.
Детальніше - на -
Пояснення:
Відповідь:
1,2,3,4 - в примечании.
Пояснення:
5. Дано:
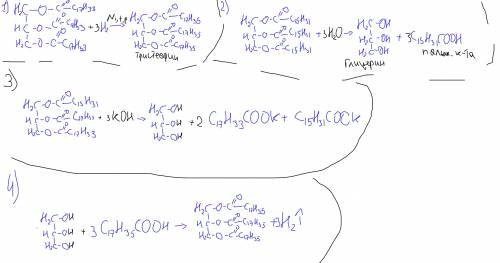
m(C₃H₈O₃)=9.2 g | (C₁₇H₃₅COO)₃C₃H₅ + H₂O →
____________________|→C₃H₈O₃ + 3C₁₈H₃₆O₂
m((C₁₇H₃₅COO)₃C₃H₅)-? | Соотношение моль → 1:1
n(C₃H₈O₃)=9.2/92=0.1 моль
n(C₃H₈O₃)=n((C₁₇H₃₅COO)₃C₃H₅)=0.1 моль
m((C₁₇H₃₅COO)₃C₃H₅)=0.1*530=53 g
6. Дано:
m(C₁₈H₃₄O₂)=64 г | 64 г - 100%
w(примесей)=12 % | х г - 100%-12% (=88%)
_______________| Х=64*88/100%=56.32 г
m(C₅₇H₁₀₄O₆)-? | 3C₁₈H₃₄O₂ +C₃H₈O₃ →→+(H₂SO₄)→→ C₅₇H₁₀₄O₆ +3 H₂O . Соотношение → 3:1
3n(C₁₈H₃₄O₂)=n(C₅₇H₁₀₄O₆)=3*m(C₁₈H₃₄O₂)/Mr(C₁₈H₃₄O₂)=3*56.32/282=0.596 моль
m(C₅₇H₁₀₄O₆)=0.596*884=526,864 g
*Поставьте лучшее
H₃C'''C₂H₅
||
HO-CH₂-C-CH-CH₂-CH₃
|
H₃C
3)Уравнения реакции
a)2C₃H₅(OH)₃+6Na=2C₃H₅(ONa)₃+3H₂
б)C₃H₅(OH)₃+3HBr=C₃H₅Br₃+3H₂O
в)C₃H₅(OH)₃+3HNO₃=C₃H₅(NO₃)₃+3H₂O
г)2C₃H₅(OH)₃+Cu(OH)₂=Cu(C₃H₅(OH)₂O)₂+2H₂O