ответ: 52.8грамм
Объяснение:
Есть известь негашеная - CaO (оксид кальция II)
А есть гашеная - Ca(OH)2 (гидроксид кальция)
Также есть известь как материал - CaO и MgO
Процесс нагревания означает реакцию разложения, то есть в выходе будут только те атомы, которые были в исходных продуктах. А во всех предложенных известях нет углерода, поэтому углекислый раз в принципе не образуется. Поэтому задача нерешаема.
НО есть известь воздушная или же мел - CaCO3, который уже подходит и делает реакцию
CaCO3→СаО+СО2↑
Если идти так, то задача крайне тривиальна, так как количество молей углекислого газа и извести совпадает. То есть n(CaCO3)=n(CO2)
n(CaCO3)=m(CaCO3)/M(CaCO3)
m(CO2)=n(CO2)*M(CO2)=n(CaCO3)*M(CO2)=m(CaCO3)/M(CaCO3)*M(CO2)=
=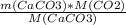 =
= =52.8 г.
=52.8 г.
Дано:
m(CaCO3)=120г.
Найти: m(CO2)
Решение расписал
маса(m)p-pa1=300г
W%1=10%=0.1
маса(m)p-pa2=250г
W%2=45%=0.45
Найти:W%3-?
Решение:маса(m)p.в.1=300*0,1=30г
маса(m)p.в.2=250*0,45=112.5г
маса(m)p.в.3=30+112.5=142.5г
маса(m)p-pa3=250+300=550г
W%3=142.5/550 *100%=26%