Для решения составляется диагональная схема: в центре пишется искомая концентрация, у левого конца каждой диагонали пишут данные концентрации. Затем по диагонали производят вычитание:
10 - 3 = 7 и 20 - 10 = 10.
Из большей части вычитают меньшую, результаты выставляют у правого конца соответствующей диагонали. Получилось, что смешать требуется 10 в.ч. 3% и 7 в.ч. 20% раствора, т.е. в соотношении 1:2.
20 7
\ /
10
/ \
3 10
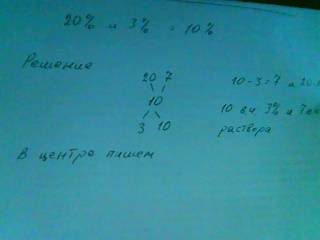
20.2 г
Объяснение:
Пишем обе реакции
2KNO₃ = 2KNO₂ + O₂ - реакция №1
2AgNO₃ = 2Ag + 2NO₂ + O₂ - реакция №2
Считаем массу кислорода в газовой смеси
m(O₂) = m(смеси) * w(O₂) = 9.4 * 0.5107 = 4.8 г (0.15 моль)
Пусть х моль - количество вещества кислорода в первой реакции, тогда 0.15 - х моль - количество вещества кислорода во второй реакции, а 2(0.15 - х) моль - количество вещества оксида азота. Поэтому
m(O₂) + m(NO₂) = M(O₂) * n(O₂) + M(NO₂) * n(NO₂) = 9.4 г
4.8 + 46 * 2 * (0.15 - x) = 9.4
x = 0.1 моль
Считаем массу нитрата калия
m(KNO₃) = n(KNO₃) * M(KNO₃) = 2n(O₂) * M(KNO₃) = 2 * 0.1 * 101 = 20.2 г
ω(C) = 10,1% или 0,101
ω(Cl) = 89,9% или 0,899
Dвозд. = 8,172
Найти:
CxCly - ?
Решение.
M(CxCly) = 29 г/моль*8,172 = 237 г/моль
m(C) = 237 г/моль*0,101 = 24 г
n(C) = m(C)/M(C) = 24 г/12 г/моль = 2 моль
m(Cl) = 237 г*0,899 = 213 г
n(Cl) = m(Cl)/M(Cl) = 213 г/35,5 г/моль = 6 моль
n(C):n(Cl) = 2:6
Следовательно, формула С2Сl6