Швидкість реакції характеризує зміну кількості речовини її компонентів (реагентів чи продуктів) за певний проміжок часу.
Нам відомо, що реакції проходили однакову кількість часу, тож швидкість реакції буде більша в тому реакторі, в якому за цей проміжок утворилася більша кількість речовини вуглекислого газу.
1 реактор:
Формула кількості речовини:
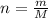
Знайдемо молярну масу вуглекислого газу:
M (CO₂) = 12 + 2 * 16 = 44 (г/моль).
Тепер знайдемо кількість речовини:
n (CO₂) = 6,6 : 44 = 0,15 (моль).
2 реактор:
Формула кількості речовини:
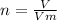
Vm (молярний об'єм) газів за нормальних умов дорівнює 22,4 л\моль.
Знайдемо кількість речовини:
n (CO₂) = 4,48 : 22,4 = 0,2 (моль).
Порівняємо кількості речовин вуглекислого газу, що виділився в першому і другому реакторах:
n₁ < n₂
Значить, в другому реакторі швидкість реакції більша.
Відповідь: у другому.
-Al,Ga,In.
-Na,Si,S.