ответ прикреплён........
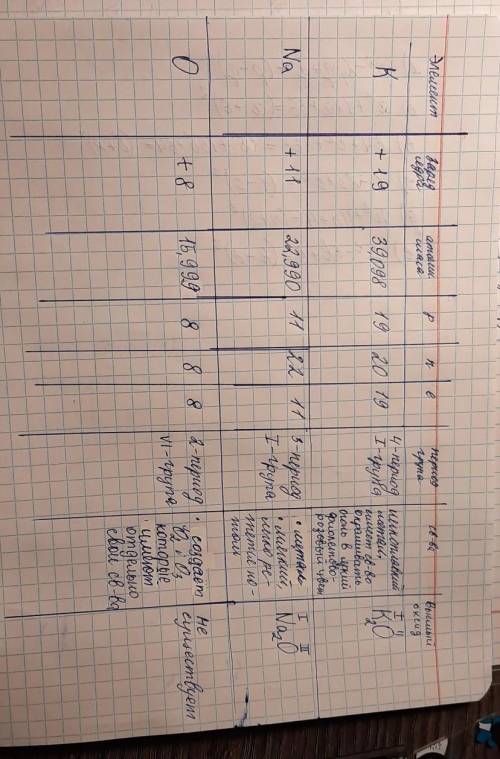
К - мягкий щелочной металл серебристо-белого цвета
Имеет свойство окрашивать открытый огонь в яркий фиолетово-розовый цвет. Калий имеет высокую химическую активность, это сильный восстановитель. При реакции с водой происходит взрыв, при длительном нахождении на воздухе полностью разрушается. Очень лёгкий и легкоплавкий.
Na - виде простого вещества представляет собой мягкий щелочной металл серебристо-белого цвета, мягкий (легко режется ножом), легкоплавкий
О - создаёт такие простые в-ва как О2 и О3
с-ва О2:газ без цвета, запаха и вкуса. Он примерно в 1,1 раза тяжелее воздуха. При температуре –183 °С кислород сжижается и превращается в голубую жидкость, а при –218 °С становится твёрдым. Кислород плохо растворяется в воде.
с-ва О3: светло-синий газ, имеет запах, t плавления: -193, t кипения: -112
Объяснение:
Обменной реакцией нельзя. Соляная кислота и её соли не реагируют с сульфатом алюминия, так как сульфат алюминия соль сильной кислоты.
Можно получить таким :
Al2(SO4)3 + 6NaOH = 2Al(OH)3 + 3Na2SO4
Сначала действуем на сульфат щелочью. Образуется нерастворимый гидроксид алюминия.
Если добавить еще щелочи, он растворится. Образуется комплексное соединение.
Al(OH)3 + NaOH = Na[ Al(OH)4 ]
Если подействовать на этот комплекс соляной кислотой, образуется хлорид алюминия.
Na[ Al(OH)4 ] + 4HCl = NaCl + AlCl3 + 4H2O
Оксиды - соединение(бинарное) химического элемента с кислородом.