Расставить коэффициенты и определить тип реакции: na + cl2 — nacl al + cl2 — а1с13 fecl2 + cl2 → fecl3 с3н6 + 02 →c02 + h20 cu + 02 → cuo fe(oh)3 →fe203 + н20 al + cubr2 → аlbr3 + сu ca(oh)2 + na3p04 → ca3(p04)2 + naoh к20 + н20→ кон n02→ no + 02 в2н6 + 02 → в2о3 + н20 с5н10 + 02→ с02 +н20 al + h2so4 →a12(s04)3 + h2 bacl2 + fe2(s04)3 → fecl3 + bas04 p205 + h20→ h3p04 mno + 02 →mn02 ph3 + 02→p205 + h20 c6h6 + 02→ c02 + h2
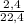 = 0,107 моль
= 0,107 моль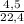 = 0,2 моль
= 0,2 моль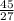 ≈ 1,7 моль
≈ 1,7 моль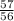 = 1,017 моль
= 1,017 моль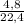 = 0,2 моль
= 0,2 моль
2Na + Cl2 —> 2NaCl - соед.
2Al + 3Cl2 —> 2А1С13 - соед.
2FeCl2 + Cl2 → 2FeCl3 - соед.
2С3Н6 +9 02 →6C02 + 6H20 - окисление
2Cu + 02 → 2CuO - соед
2Fe(OH)3 →Fe203 + 3Н20 - разл.
2Al + 3CuBr2 → 2АlBr3 + 3Сu - замещ.
3Ca(OH)2 + 2Na3P04 → Ca3(P04)2 + 6NaOH - обмен
К20 + Н20→ 2КОН - соед.
2N02→ 2NO + 02 - разл.
В2Н6 + 302 → В2О3 +3Н20 - окисление
2С5Н10 + 1502→ 10С02 +10Н20 - окисление
2Al + 3H2SO4 →A12(S04)3 + 3H2 - замещ.
3BaCl2 + 3Fe2(S04)3 → 2FeCl3 +3 BaS04 - обмен
P205 + 3H20→ 2H3P04 - соед.
2MnO + 02 →2Mn02 - соед.
2PH3 + 402→P205 + 3H20 - окисление
2C6H6 + 1502→ 12C02 + 6H2O - окисление