В термодинамических неравновесных системах возникают особые необратимые процессы, в результате которых происходит пространственный перенос энергии, массы и импульса.
Если газ находится в состоянии равновесия, макроскопические параметры в различных частях системы одинаковы. Однако если в произвольной части системы один из параметров изменился, т. е. система стала неравновесной, возникнут процессы, стремящиеся вернуть систему в равновесное состояние, и эти процессы называют явлением переноса.
В зависимости от того, какой параметр изменяется, различают
1) теплопроводность — перенос энергии
2) диффузия — перенос массы
3) вязкость (или внутреннее трение) — перенос импульса.
Дано:
dT=300 град. Цельсия=300 К.
V2=2V1;
T1=?
______
Решение:
Для начала запомни:
Изохорный процесс : процесс происходящий при неизменном объеме. (V=const).
Изобарный процесс: процесс происходящий при неизменном давлении. (P=const).
Изотермический процесс: процесс происходящий при неизменной температуре. (T=const).
То есть, у нас изобарный процесс: P1=P2=P;
Теперь, запишем уравнение Менделеева - Клапейрона: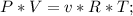
Где P - давление, V - объем газа, v - молярная масса газа, R - универсальная газовая постоянная, равная 8,31 Дж/К*моль; T - температура газа.
Теперь запишем для двух наших случаев: (Учитывая, что процесс изобраный).
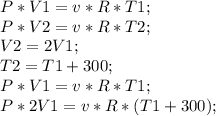
Делим первое уравнение на второе: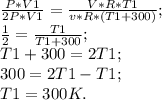
Получили, что начальная температура газа равна 300 К. (Ну или переводя в Цельсии: 300-273=27 град С).
ответ: T1=300 К.
2) Q1=mc(t2-t1)
3) Q2=mλ
4) Q3=m1q
5) mc(t2-t1)+mλ=m1q
6) m(c(t2+t1)+λ)=m1q
7) m=(c(t2+t1)+λ)/m1q - ответ.