х г 12 л
106 г 22,4 л
1. Знайдемо чисту масу кальцинованої соди:
при взаємодіїї 106 г соди віділяється 22,4 л вуглекислого газу, а
при -- // -- х г_________________12 л, звідки
х=106*12/22,4=57 г
2. Тепер,віднявши від загальної маси зразка отриману чисту масу соди,отримаємо масу домішків:
m(домішків)=m(зразка) - m(Na2CO3)=68 - 57 =11 г
3. Віднесемо масу домішків до загальної маси зразка і отримаємо масову частку домішків:
w(домішків)=m(домішків)/m(зразка)=11/68=0,16 або 16%
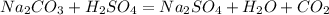
2As + 3O₂ = 2As₂O₃
М(2As) = 75 + 75 = 150 г/моль (это мы узнаем из таблицы Менделеева).
М(3O₂) = 2(16+16+16) = 96 г/моль (это мы узнаем из таблицы Менделеева).
m(2As) = 900г (это написано в условии).
m(3O₂) = x.
Составим пропорцию.
900:150=х:96
х=576 г.
ответ: m(3O₂) = 576 г.